42 pada tabel periodik. Sistem periodik Mendeleev. Unsur kimia dari tabel periodik
Tabel periodik unsur kimia adalah klasifikasi unsur kimia yang dibuat oleh D.I. Mendeleev berdasarkan hukum periodik yang ditemukannya pada tahun 1869.
D.I.Mendeleev
Menurut rumusan modern hukum ini, dalam rangkaian unsur-unsur yang tersusun secara terus-menerus menurut kenaikan besarnya muatan positif inti atomnya, unsur-unsur dengan sifat serupa berulang secara berkala.
Tabel periodik unsur kimia yang disajikan dalam bentuk tabel terdiri dari periode, deret, dan golongan.
Pada awal setiap periode (kecuali periode pertama), unsur tersebut telah menyatakan sifat logam (logam alkali).

Simbol untuk tabel warna: 1 - tanda kimia suatu unsur; 2 - nama; 3 - massa atom (berat atom); 4 - nomor seri; 5 - distribusi elektron melintasi lapisan.
Dengan bertambahnya nomor atom suatu unsur, sama dengan muatan positif inti atomnya, sifat logam secara bertahap melemah dan sifat non-logam meningkat. Unsur kedua dari belakang pada setiap periode adalah unsur dengan sifat non-logam (), dan yang terakhir adalah gas inert. Pada periode I terdapat 2 unsur, pada II dan III - 8 unsur, pada IV dan V - 18, pada VI - 32 dan pada VII (belum selesai periode) - 17 unsur.
Tiga periode pertama disebut periode kecil, masing-masing terdiri dari satu baris mendatar; sisanya - dalam periode besar, yang masing-masing (kecuali periode VII) terdiri dari dua baris horizontal - genap (atas) dan ganjil (bawah). Hanya logam yang ditemukan dalam barisan genap dengan periode yang besar. Sifat-sifat unsur dalam deret ini sedikit berubah seiring bertambahnya nomor urut. Sifat-sifat unsur pada barisan ganjil periode besar berubah. Pada periode VI, lantanum diikuti oleh 14 unsur yang sifat kimianya sangat mirip. Unsur-unsur ini, yang disebut lantanida, dicantumkan secara terpisah di bawah tabel utama. Aktinida, unsur-unsur setelah aktinium, disajikan serupa dalam tabel.

Tabel ini memiliki sembilan grup vertikal. Nomor golongan, dengan pengecualian yang jarang, sama dengan valensi positif tertinggi dari unsur-unsur golongan ini. Setiap kelompok, kecuali kelompok nol dan kedelapan, dibagi menjadi beberapa subkelompok. - utama (terletak di sebelah kanan) dan sekunder. Pada subkelompok utama, dengan bertambahnya nomor atom, sifat logam suatu unsur menjadi lebih kuat dan sifat nonlogam melemah.
Dengan demikian, sifat kimia dan sifat fisik suatu unsur ditentukan oleh tempat yang ditempati suatu unsur dalam tabel periodik.
Unsur biogenik, yaitu unsur yang merupakan bagian dari organisme dan menjalankan peran biologis tertentu di dalamnya, menempati bagian atas Tabel periodik. Sel yang ditempati oleh unsur-unsur penyusun sebagian besar (lebih dari 99%) materi hidup berwarna biru, in berwarna merah muda- sel ditempati oleh unsur mikro (lihat).
Tabel periodik unsur kimia adalah pencapaian terbesar ilmu pengetahuan alam modern dan ekspresi jelas dari hukum alam dialektis yang paling umum.
Lihat juga, Berat atom.
Sistem periodik unsur kimia adalah klasifikasi alami unsur kimia yang dibuat oleh D. I. Mendeleev berdasarkan hukum periodik yang ditemukannya pada tahun 1869.
Dalam rumusan aslinya, hukum periodik D.I. Mendeleev menyatakan: sifat-sifat unsur kimia, serta bentuk dan sifat senyawanya, secara periodik bergantung pada berat atom unsur-unsur tersebut. Selanjutnya, dengan berkembangnya doktrin struktur atom, ditunjukkan bahwa ciri yang lebih akurat dari setiap unsur bukanlah berat atom (lihat), tetapi nilai muatan positif inti atom unsur tersebut, sama dengan nomor urut (atom) unsur ini dalam sistem periodik D. I. Mendeleev . Jumlah muatan positif pada inti atom sama dengan jumlah elektron yang mengelilingi inti atom, karena atom secara keseluruhan netral secara listrik. Berdasarkan data tersebut, hukum periodik dirumuskan sebagai berikut: sifat-sifat unsur kimia, serta bentuk dan sifat senyawanya, secara periodik bergantung pada besarnya muatan positif inti atomnya. Artinya, dalam rangkaian unsur-unsur yang tersusun berurutan berdasarkan kenaikan muatan positif inti atomnya, unsur-unsur yang mempunyai sifat serupa akan berulang secara berkala.
Bentuk tabel tabel periodik unsur kimia disajikan di dalamnya bentuk modern. Terdiri dari periode, deret, dan grup. Suatu periode mewakili serangkaian elemen horizontal berturut-turut yang disusun berdasarkan peningkatan muatan positif inti atomnya.
Pada awal setiap periode (kecuali periode pertama) terdapat unsur dengan sifat logam yang jelas (logam alkali). Kemudian, seiring bertambahnya nomor urut, sifat logam unsur-unsur tersebut berangsur-angsur melemah dan sifat non-logam meningkat. Unsur kedua dari belakang pada setiap periode adalah unsur dengan sifat non-logam (halogen), dan yang terakhir adalah gas inert. Periode pertama terdiri dari dua unsur, peran logam alkali dan halogen di sini secara bersamaan dilakukan oleh hidrogen. Periode II dan III masing-masing terdiri dari 8 unsur yang disebut tipikal oleh Mendeleev. Periode IV dan V masing-masing mengandung 18 unsur, VI-32. Periode VII belum selesai dan sedang diisi ulang secara artifisial elemen yang dibuat; Saat ini terdapat 17 unsur dalam periode ini. Periode I, II dan III disebut kecil, masing-masing terdiri dari satu baris horizontal, IV-VII besar: (kecuali VII) mencakup dua baris horizontal - genap (atas) dan ganjil (bawah). Dalam barisan genap periode besar hanya terdapat logam, dan perubahan sifat-sifat unsur dalam barisan dari kiri ke kanan dinyatakan lemah.
Pada deret ganjil periode besar, sifat-sifat unsur dalam deret tersebut berubah sama seperti sifat-sifat unsur tipikal. Pada baris genap periode VI, setelah lantanum, terdapat 14 unsur [disebut lantanida (lihat), lantanida, unsur tanah jarang], yang sifat kimianya mirip dengan lantanum dan satu sama lain. Daftarnya diberikan secara terpisah di bawah tabel.
Unsur-unsur yang mengikuti aktinium - aktinida (aktinida) - dicantumkan secara terpisah dan dicantumkan di bawah tabel.
Dalam tabel periodik unsur kimia, sembilan golongan disusun secara vertikal. Nomor golongan sama dengan valensi positif tertinggi (lihat) dari unsur-unsur golongan tersebut. Pengecualian adalah fluor (hanya dapat bersifat monovalen negatif) dan brom (tidak dapat bersifat heptavalen); selain itu, tembaga, perak, emas dapat menunjukkan valensi lebih besar dari +1 (Cu-1 dan 2, Ag dan Au-1 dan 3), dan dari unsur golongan VIII, hanya osmium dan rutenium yang memiliki valensi +8 . Setiap kelompok, kecuali kelompok kedelapan dan nol, dibagi menjadi dua subkelompok: subkelompok utama (terletak di sebelah kanan) dan subkelompok sekunder. Subkelompok utama mencakup unsur-unsur khas dan unsur-unsur periode panjang, subkelompok sekunder hanya mencakup unsur-unsur periode panjang dan, terlebih lagi, logam.
Dilihat dari sifat kimianya, unsur-unsur dari setiap subkelompok suatu golongan tertentu berbeda secara signifikan satu sama lain, dan hanya valensi positif tertinggi yang sama untuk semua unsur dalam suatu golongan tertentu. Dalam subkelompok utama, dari atas ke bawah, sifat logam suatu unsur diperkuat dan sifat non-logam melemah (misalnya, fransium adalah unsur dengan sifat logam paling menonjol, dan fluor adalah non-logam). Dengan demikian, kedudukan suatu unsur dalam sistem periodik Mendeleev (bilangan urut) menentukan sifat-sifatnya, yaitu rata-rata sifat-sifat unsur tetangganya secara vertikal dan horizontal.
Beberapa kelompok unsur mempunyai nama khusus. Jadi, unsur-unsur dari subkelompok utama golongan I disebut logam alkali, golongan II - logam alkali tanah, golongan VII - halogen, unsur-unsur yang terletak di belakang uranium - transuranium. Unsur-unsur yang menjadi bagian organisme, ikut serta dalam proses metabolisme dan mempunyai peranan biologis yang jelas disebut unsur biogenik. Semuanya menempati bagian atas tabel D.I. Ini terutama adalah O, C, H, N, Ca, P, K, S, Na, Cl, Mg dan Fe, yang merupakan sebagian besar materi hidup (lebih dari 99%). Tempat yang ditempati unsur-unsur ini dalam tabel periodik berwarna biru muda. Unsur biogenik, yang jumlahnya sangat sedikit di dalam tubuh (dari 10 -3 hingga 10 -14%), disebut unsur mikro (lihat). Dalam sel sistem periodik, diwarnai kuning, ditempatkan elemen mikro, penting penting yang telah terbukti pada manusia.
Menurut teori struktur atom (lihat Atom), sifat kimia suatu unsur terutama bergantung pada jumlah elektron pada kulit elektron terluar. Perubahan periodik sifat-sifat unsur dengan bertambahnya muatan positif inti atom dijelaskan oleh pengulangan periodik struktur kulit elektron terluar (tingkat energi) atom.
Dalam periode kecil, dengan peningkatan muatan positif inti, jumlah elektron pada kulit terluar meningkat dari 1 menjadi 2 pada periode I dan dari 1 menjadi 8 pada periode II dan III. Oleh karena itu terjadi perubahan sifat-sifat unsur dalam periode dari logam alkali menjadi gas inert. Kulit elektron terluar, yang mengandung 8 elektron, lengkap dan stabil secara energi (elemen golongan nol bersifat inert secara kimia).
Dalam periode yang lama dalam barisan genap, seiring dengan bertambahnya muatan positif inti, jumlah elektron pada kulit terluar tetap konstan (1 atau 2) dan kulit terluar kedua terisi elektron. Oleh karena itu lambatnya perubahan sifat-sifat unsur dalam baris genap. Dalam rangkaian periode besar yang ganjil, seiring dengan bertambahnya muatan inti, kulit terluar terisi elektron (dari 1 hingga 8) dan sifat-sifat unsur berubah dengan cara yang sama seperti sifat-sifat unsur pada umumnya.
Jumlah kulit elektron dalam suatu atom sama dengan nomor periode. Atom unsur-unsur subkelompok utama memiliki jumlah elektron pada kulit terluarnya sama dengan nomor golongan. Atom unsur subkelompok samping mengandung satu atau dua elektron di kulit terluarnya. Hal ini menjelaskan perbedaan sifat unsur-unsur subkelompok utama dan sekunder. Nomor golongan menunjukkan kemungkinan jumlah elektron yang dapat ikut serta dalam pembentukan ikatan kimia (valensi) (lihat Molekul), oleh karena itu elektron tersebut disebut valensi. Untuk unsur-unsur subkelompok samping, tidak hanya elektron pada kulit terluar yang bervalensi, tetapi juga elektron pada kulit kedua dari belakang. Jumlah dan struktur kulit elektron ditunjukkan dalam tabel periodik unsur kimia terlampir.
Hukum periodik D. I. Mendeleev dan sistem yang didasarkan padanya hanya memiliki nilai yang besar dalam sains dan praktik. Hukum dan sistem periodik menjadi dasar penemuan unsur-unsur kimia baru, penentuan berat atom secara tepat, pengembangan doktrin struktur atom, penetapan hukum geokimia distribusi unsur-unsur di kerak bumi dan bumi. perkembangan gagasan modern tentang makhluk hidup, yang komposisi dan pola yang terkait dengannya sesuai dengan sistem periodik. Aktivitas biologis unsur-unsur dan kandungannya dalam tubuh juga sangat ditentukan oleh tempatnya dalam tabel periodik Mendeleev. Jadi, dengan bertambahnya nomor urut pada beberapa golongan, maka toksisitas suatu unsur meningkat dan kandungannya dalam tubuh menurun. Hukum periodik merupakan ekspresi jelas dari hukum dialektis paling umum dari perkembangan alam.
TABEL PERIODIK MENDELEEV
Konstruksi jawaban tabel periodik unsur kimia Mendeleev periode karakteristik teori bilangan dan basis ortogonal. Penambahan matriks Hadamard dengan matriks orde genap dan ganjil menciptakan dasar struktural elemen matriks bersarang: matriks orde pertama (Odin), kedua (Euler), ketiga (Mersenne), keempat (Hadamard) dan kelima (Fermat).
Sangat mudah untuk melihat bahwa ada 4 pesanan k Matriks Hadamard sesuai dengan unsur inert dengan massa atom kelipatan empat: helium 4, neon 20, argon 40 (39.948), dll., tetapi juga dasar-dasar kehidupan dan teknologi digital: karbon 12, oksigen 16, silikon 28 , Jerman 72.
Tampaknya dengan matriks Mersenne orde 4 k–1, sebaliknya, segala sesuatu yang aktif, beracun, merusak dan korosif saling berhubungan. Tapi ini juga merupakan unsur radioaktif - sumber energi, dan timbal 207 (produk akhir, garam beracun). Fluor, tentu saja, adalah 19. Urutan matriks Mersenne sesuai dengan urutan unsur radioaktif yang disebut deret aktinium: uranium 235, plutonium 239 (isotop yang merupakan sumber energi atom lebih kuat daripada uranium), dll. Ini juga merupakan logam alkali litium 7, natrium 23 dan kalium 39.

Gallium – berat atom 68
Pesanan 4 k–2 Matriks Euler (Mersenne ganda) berhubungan dengan nitrogen 14 (dasar atmosfer). Garam meja dibentuk oleh dua atom “mirip mersenne” yaitu natrium 23 dan klor 35; bersama-sama kombinasi ini merupakan karakteristik matriks Euler. Klorin yang lebih masif dengan berat 35,4 kurang dari dimensi Hadamard 36. Kristal garam meja: kubus (! yaitu karakter pendiam, Hadamarov) dan segi delapan (lebih menantang, tidak diragukan lagi ini adalah Euler).
Dalam fisika atom, besi transisi 56 - nikel 59 merupakan batas antar unsur yang menyediakan energi selama sintesis inti yang lebih besar (bom hidrogen) dan peluruhan (bom uranium). Orde 58 terkenal karena tidak hanya tidak memiliki analogi matriks Hadamard berupa matriks Belevich dengan nol pada diagonalnya, juga tidak banyak matriks berbobot - ortogonal terdekat W(58,53) memiliki 5 angka nol di setiap kolom dan baris (celah dalam).
Dalam deret yang sesuai dengan matriks Fermat dan substitusinya pada orde 4 k+1, atas kehendak takdir, harganya Fermium 257. Anda tidak bisa mengatakan apa-apa, tepat sasaran. Di sini ada emas 197. Tembaga 64 (63.547) dan perak 108 (107.868), simbol elektronik, tampaknya tidak mencapai emas dan sesuai dengan matriks Hadamard yang lebih sederhana. Tembaga, dengan berat atom tidak jauh dari 63, aktif secara kimia - oksida hijaunya sudah dikenal luas.
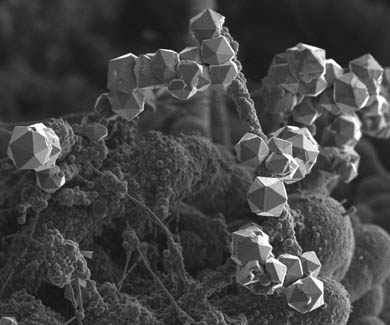
Kristal boron dengan pembesaran tinggi
DENGAN rasio emas boron terikat - massa atom di antara semua unsur lainnya paling dekat dengan 10 (lebih tepatnya 10,8, kedekatan berat atom dengan bilangan ganjil juga berpengaruh). Boron adalah elemen yang agak rumit. Boron memainkan peran yang rumit dalam sejarah kehidupan itu sendiri. Struktur kerangka pada strukturnya jauh lebih kompleks daripada pada struktur berlian. Jenis ikatan kimia unik yang memungkinkan boron menyerap pengotor apa pun masih sangat kurang dipahami, meskipun penelitian terkait dengannya jumlah besar ilmuwan telah menerima Hadiah Nobel. Bentuk kristal boron adalah ikosahedron, dengan lima segitiga membentuk puncaknya.
Misteri Platinum. Unsur kelima tidak diragukan lagi adalah logam mulia seperti emas. Superstruktur di atas dimensi Hadamard 4 k, 1 besar.

Isotop stabil uranium 238
Namun perlu diingat bahwa bilangan Fermat jarang ditemukan (yang paling mendekati adalah 257). Kristal emas asli bentuknya mendekati kubus, namun pentagramnya juga berkilau. Tetangga terdekatnya, platina, suatu logam mulia, berjarak kurang dari 4 berat atom dari emas 197. Platinum memiliki berat atom bukan 193, tetapi sedikit lebih tinggi, 194 (urutan matriks Euler). Ini adalah hal kecil, tetapi itu membawanya ke dalam kelompok elemen yang lebih agresif. Perlu diingat, karena kelembamannya (mungkin larut dalam aqua regia), platina digunakan sebagai katalis aktif. proses kimia.
Platina spons membakar hidrogen pada suhu kamar. Karakter platina sama sekali tidak damai; iridium 192 (campuran isotop 191 dan 193) berperilaku lebih damai. Ini lebih mirip tembaga, tetapi dengan bobot dan karakter emas.
Di antara neon 20 dan natrium 23 tidak ada unsur dengan berat atom 22. Tentu saja, berat atom merupakan suatu sifat yang tidak terpisahkan. Namun di antara isotop, pada gilirannya, terdapat juga korelasi sifat yang menarik dengan sifat bilangan dan matriks basa ortogonal yang sesuai. Bahan bakar nuklir yang paling banyak digunakan adalah isotop uranium 235 (urutan matriks Mersenne), yang memungkinkan terjadinya reaksi berantai nuklir berkelanjutan. Di alam, unsur ini terdapat dalam bentuk stabil uranium 238 (ordo matriks Euler). Tidak ada unsur dengan berat atom 13. Sedangkan untuk chaos, terbatasnya jumlah unsur stabil dalam tabel periodik dan sulitnya menemukan matriks tingkat orde tinggi karena penghalang yang diamati pada matriks orde ketigabelas saling berkorelasi.
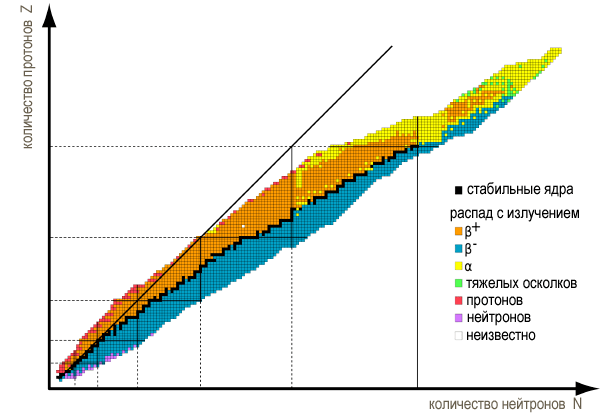
Isotop unsur kimia, pulau stabilitas
Eter dalam tabel periodik
Tabel periodik unsur kimia yang secara resmi diajarkan di sekolah dan universitas adalah sebuah pemalsuan. Mendeleev sendiri, dalam karyanya yang berjudul “An Attempt at a Chemical Understanding of the World Ether”, memberikan tabel yang sedikit berbeda (Museum Politeknik, Moskow):

Terakhir kali Tabel Periodik yang sebenarnya diterbitkan dalam bentuk yang tidak terdistorsi adalah pada tahun 1906 di St. Petersburg (buku teks “Fundamentals of Chemistry”, edisi VIII). Perbedaannya terlihat: golongan nol telah dipindahkan ke golongan ke-8, dan unsur yang lebih ringan dari hidrogen, yang menjadi awal tabel dan yang secara konvensional disebut Newtonium (eter), sepenuhnya dikecualikan.

Meja yang sama diabadikan oleh Kamerad “tiran berdarah”. Stalin di St.Petersburg, Moskovsky Avenue. 19. VNIIM im. D. I. Mendeleeva (Institut Penelitian Metrologi Seluruh Rusia)
Tabel Monumen Tabel periodik unsur kimia D.I. Mendeleev membuat mosaik di bawah bimbingan Profesor Akademi Seni V.A. Frolov (desain arsitektur oleh Krichevsky). Monumen ini didasarkan pada tabel dari Fundamentals of Chemistry edisi ke-8 masa lalu (1906) karya D.I. Mendeleev. Unsur-unsur yang ditemukan selama kehidupan D.I. Mendeleev ditandai dengan warna merah. Elemen ditemukan dari tahun 1907 hingga 1934 , ditunjukkan dengan warna biru. Ketinggian meja tugu adalah 9 m, luas totalnya adalah 69 m persegi. M
.jpg)
Mengapa dan bagaimana mereka bisa berbohong kepada kita secara terbuka?
Tempat dan peran eter dunia dalam tabel sebenarnya D.I. Mendeleev
1. Suprema lex – salus populi
Banyak yang telah mendengar tentang Dmitry Ivanovich Mendeleev dan tentang “Hukum Periodik Perubahan Sifat Unsur Kimia dalam Golongan dan Deret” yang ia temukan pada abad ke-19 (1869) (nama penulis untuk tabel tersebut adalah “Sistem Periodik Unsur dalam Grup dan Seri”).
Banyak juga yang mendengar bahwa D.I. Mendeleev adalah penyelenggara dan pemimpin tetap (1869-1905) dari asosiasi ilmiah publik Rusia yang disebut “Masyarakat Kimia Rusia” (sejak 1872 - “Masyarakat Fisika-Kimia Rusia”), yang sepanjang keberadaannya menerbitkan jurnal terkenal di dunia ZhRFKhO, hingga sampai likuidasi Perkumpulan dan jurnalnya oleh Akademi Ilmu Pengetahuan Uni Soviet pada tahun 1930.
Namun hanya sedikit orang yang mengetahui bahwa D.I. Mendeleev adalah salah satu ilmuwan Rusia terakhir yang terkenal di dunia pada akhir abad ke-19 yang membela gagasan eter sebagai entitas substansial universal dalam sains dunia, yang memberinya signifikansi ilmiah dan terapan yang mendasar dalam mengungkap rahasia Keberadaan dan untuk meningkatkan kehidupan ekonomi masyarakat.
Bahkan lebih sedikit lagi yang mengetahui bahwa setelah kematian mendadak (!!?) D.I. Mendeleev (27/01/1907), yang kemudian diakui sebagai ilmuwan terkemuka oleh semua komunitas ilmiah di seluruh dunia kecuali Akademi Ilmu Pengetahuan St. Petersburg, penemuan utamanya - "Hukum Periodik" - sengaja dan luas dipalsukan oleh ilmu pengetahuan akademis dunia .
Dan sangat sedikit orang yang mengetahui bahwa semua hal di atas dihubungkan oleh benang pengorbanan para wakil terbaik dan pengemban Pikiran Fisik Rusia yang abadi demi kebaikan rakyat, kemaslahatan umum, meskipun gelombang tidak bertanggung jawab semakin meningkat. di lapisan masyarakat tertinggi saat itu.
Intinya, disertasi ini dikhususkan untuk pengembangan menyeluruh dari tesis terakhir, karena dalam sains sejati, pengabaian terhadap faktor-faktor esensial selalu membawa hasil yang salah. Jadi pertanyaannya adalah: mengapa para ilmuwan berbohong?
2. Faktor Psik: ni foi, ni loi
Baru sekarang, sejak akhir abad ke-20, masyarakat mulai memahami (bahkan dengan malu-malu) contoh praktis bahwa seorang ilmuwan yang luar biasa dan berkualifikasi tinggi, tetapi tidak bertanggung jawab, sinis, tidak bermoral dengan “reputasi dunia” tidak kalah berbahayanya bagi masyarakat dibandingkan dengan seorang politisi, militer, pengacara, atau, paling banter, seorang bandit jalan raya yang “luar biasa” tetapi tidak bermoral .
Masyarakat ditanamkan gagasan bahwa komunitas ilmiah akademis dunia adalah kasta makhluk surgawi, biksu, bapa suci yang peduli siang dan malam terhadap kesejahteraan masyarakat. Dan manusia biasa harus memandang langsung para dermawan mereka, dengan patuh mendanai dan melaksanakan semua proyek, ramalan, dan instruksi “ilmiah” mereka untuk mengatur kembali kehidupan publik dan pribadi mereka.
Faktanya, unsur kriminal dalam komunitas ilmiah dunia tidak kalah pentingnya dengan politisi yang sama. Selain itu, tindakan kriminal dan anti-sosial yang dilakukan oleh para politisi seringkali langsung terlihat, namun tindakan kriminal dan berbahaya, namun “berbasis ilmiah” dari para ilmuwan “terkemuka” dan “otoritatif” tidak langsung dikenali oleh masyarakat, tetapi setelah bertahun-tahun, atau bahkan puluhan tahun, di “kulit publik” miliknya sendiri.
Mari kita lanjutkan studi kita tentang faktor psikofisiologis aktivitas ilmiah yang sangat menarik (dan rahasia!) ini (sebut saja faktor psi), yang menghasilkan hasil negatif yang tidak terduga (?!) secara a posteriori: “kami ingin apa yang terbaik bagi orang-orang, tapi ternyata seperti biasa, itu. merugikan." Memang dalam sains, akibat negatif juga merupakan akibat yang tentunya memerlukan pemahaman ilmiah yang komprehensif.
Mengingat korelasi antara faktor psi dan fungsi tujuan utama (BTF) dari badan pendanaan negara, kami sampai pada kesimpulan yang menarik: apa yang disebut sebagai ilmu pengetahuan yang murni dan besar pada abad-abad yang lalu kini telah merosot menjadi kasta yang tak tersentuh, yaitu. ke dalam kotak tertutup para tabib istana yang dengan cemerlang menguasai ilmu penipuan, dengan cemerlang menguasai ilmu menganiaya para pembangkang dan ilmu tunduk pada pemodal mereka yang kuat.
Perlu diingat bahwa, pertama, dalam semua yang disebut “negara-negara beradab” yang mereka sebut. “Akademi Ilmu Pengetahuan Nasional” secara formal berstatus organisasi negara dengan hak sebagai badan ahli ilmiah terkemuka dari pemerintah terkait. Kedua, semua akademi ilmu pengetahuan nasional ini disatukan menjadi satu struktur hierarki yang kaku (yang nama aslinya tidak diketahui dunia), mengembangkan satu struktur hierarki yang kaku. akademi nasional strategi ilmu pengetahuan tentang perilaku di dunia dan apa yang disebut terpadu. paradigma keilmuan yang intinya bukanlah penyingkapan hukum-hukum eksistensi, melainkan faktor psi: dengan melakukan apa yang disebut kedok “ilmiah” (demi kredibilitas) sebagai “penyembuh pengadilan” dari segala hal yang tidak wajar. tindakan mereka yang berkuasa di mata masyarakat, untuk mendapatkan kemuliaan para pendeta dan nabi, mempengaruhi, seperti seorang demiurge, jalannya sejarah manusia.
Segala sesuatu yang disebutkan di atas pada bagian ini, termasuk istilah “faktor psi” yang kami perkenalkan, telah diprediksi dengan sangat akurat dan dapat dibenarkan oleh D.I. Mendeleev lebih dari 100 tahun yang lalu (lihat, misalnya, artikel analitisnya pada tahun 1882 “Akademi seperti apa yang dibutuhkan di Rusia?”, di mana Dmitry Ivanovich sebenarnya memberikan penjelasan rinci tentang faktor psi dan di mana mereka mengusulkan sebuah program untuk reorganisasi radikal dari perusahaan ilmiah tertutup yang terdiri dari anggota Akademi Ilmu Pengetahuan Rusia yang memandang Akademi semata-mata sebagai tempat mencari makan untuk memuaskan kepentingan egois mereka.
Dalam salah satu suratnya 100 tahun yang lalu kepada profesor Universitas Kyiv P.P. Alekseev D.I. Mendeleev dengan jujur mengakui bahwa dia “siap membakar dirinya sendiri dupa untuk mengusir setan, dengan kata lain, untuk mengubah fondasi akademi menjadi sesuatu yang baru, Rusia, miliknya sendiri, cocok untuk semua orang pada umumnya dan, khususnya, untuk gerakan ilmiah di Rusia.”
Seperti yang bisa kita lihat, seorang ilmuwan, warga negara, dan patriot yang benar-benar hebat di tanah airnya mampu membuat ramalan ilmiah jangka panjang yang paling rumit sekalipun. Sekarang mari kita perhatikan aspek historis dari perubahan faktor psi yang ditemukan oleh D.I. Mendeleev pada akhir abad ke-19.
3. Fin de siècle
Sejak paruh kedua abad ke-19 di Eropa, di tengah gelombang “liberalisme,” telah terjadi pertumbuhan pesat dalam jumlah kaum intelektual, tenaga ilmiah dan teknis, serta peningkatan kuantitatif dalam teori, gagasan, dan proyek ilmiah dan teknis yang ditawarkan oleh negara-negara Eropa. personel ini kepada masyarakat.
Pada akhir abad ke-19, persaingan untuk mendapatkan “tempat di bawah sinar matahari” semakin meningkat tajam di antara mereka, yaitu. untuk gelar, penghargaan dan penghargaan, dan sebagai konsekuensi dari kompetisi ini, polarisasi personel ilmiah menurut kriteria moral semakin meningkat. Ini berkontribusi pada aktivasi faktor psi yang eksplosif.
Antusiasme revolusioner dari para ilmuwan dan intelektual muda, ambisius dan tidak berprinsip, mabuk oleh pembelajaran cepat mereka dan keinginan tidak sabar untuk menjadi terkenal dengan cara apa pun di dunia ilmiah, melumpuhkan tidak hanya perwakilan dari lingkaran ilmuwan yang lebih bertanggung jawab dan jujur, tetapi juga juga seluruh komunitas ilmiah secara keseluruhan, dengan infrastruktur dan tradisi mapan yang sebelumnya menghalangi pertumbuhan faktor psi yang tak terkendali.
Para intelektual revolusioner abad ke-19, para pengguling takhta dan sistem pemerintahan di negara-negara Eropa, memperluas metode gangster dalam perjuangan ideologis dan politik mereka melawan “orde lama” dengan bantuan bom, pistol, racun dan konspirasi) juga ke dalam bidang politik. kegiatan ilmiah dan teknis. Di ruang kelas siswa, laboratorium dan simposium ilmiah, mereka mengolok-olok akal sehat yang dianggap ketinggalan jaman, konsep logika formal yang dianggap ketinggalan jaman - konsistensi penilaian, validitasnya. Oleh karena itu, pada awal abad ke-20, alih-alih menggunakan metode persuasi, metode penindasan total terhadap lawan-lawan mereka, melalui kekerasan mental, fisik, dan moral terhadap mereka, memasuki gaya perdebatan ilmiah (atau lebih tepatnya, meledak dengan sebuah perdebatan ilmiah). memekik dan mengaum). Pada saat yang sama, tentu saja, nilai faktor psi mencapai tingkat yang sangat tinggi, mengalami titik ekstrimnya di tahun 30an.
Akibatnya, pada awal abad ke-20, kaum intelektual yang “tercerahkan” justru melakukan kekerasan, yaitu. revolusioner, dengan cara yang menggantikan paradigma ilmiah humanisme, pencerahan dan manfaat sosial dalam ilmu pengetahuan alam dengan paradigma relativisme permanennya sendiri, memberinya bentuk pseudoscientific dari teori relativitas universal (sinisme!).
Paradigma pertama mengandalkan pengalaman dan penilaian komprehensifnya untuk mencari kebenaran, mencari dan memahami hukum alam yang objektif. Paradigma kedua menekankan kemunafikan dan ketidakjujuran; dan bukan untuk mencari hukum alam yang obyektif, melainkan demi kepentingan kelompoknya yang egois hingga merugikan masyarakat. Paradigma pertama bertujuan untuk kepentingan publik, sedangkan paradigma kedua tidak berarti demikian.
Sejak tahun 1930-an hingga saat ini, faktor psi telah stabil dan tetap berada pada tingkat yang lebih tinggi dibandingkan nilainya pada awal dan pertengahan abad ke-19.
Untuk penilaian yang lebih obyektif dan jelas tentang kontribusi nyata, dan bukan mitos, dari aktivitas komunitas ilmiah dunia (diwakili oleh semua akademi sains nasional) terhadap kehidupan publik dan pribadi masyarakat, kami memperkenalkan konsep psi yang dinormalisasi. faktor.
Nilai normalisasi faktor psi sama dengan satu sesuai dengan probabilitas seratus persen untuk memperoleh hasil negatif (yaitu kerugian sosial) dari pelaksanaan pengembangan ilmu pengetahuan yang secara apriori menyatakan hasil positif (yaitu manfaat sosial tertentu) untuk satu periode waktu sejarah (perubahan satu generasi manusia, sekitar 25 tahun), di mana seluruh umat manusia mati total atau merosot dalam waktu tidak lebih dari 25 tahun sejak diperkenalkannya blok program ilmiah tertentu.
4. Bunuh dengan kebaikan
Kemenangan kejam dan kotor dari relativisme dan ateisme militan dalam mentalitas komunitas ilmiah global pada awal abad ke-20 - alasan utama dari semua masalah manusia di zaman “atom”, “kosmik” yang disebut “ kemajuan ilmu pengetahuan dan teknologi" Mari kita lihat ke belakang - bukti apa lagi yang kita perlukan saat ini untuk memahami hal yang sudah jelas: di abad ke-20 tidak ada satu pun tindakan yang bermanfaat secara sosial dari persaudaraan ilmuwan sedunia di bidang ilmu alam dan sosial yang dapat memperkuat populasi Homo sapiens , secara filogenetik dan moral. Namun yang terjadi justru sebaliknya: mutilasi tanpa ampun, perusakan dan perusakan sifat psiko-somatik seseorang, gaya hidup sehat dan habitatnya dengan berbagai dalih yang masuk akal.
Pada awal abad ke-20, semua posisi akademis utama dalam mengelola kemajuan penelitian, topik, pendanaan kegiatan ilmiah dan teknis, dll. ditempati oleh “persaudaraan orang-orang yang berpikiran sama” yang menganut agama ganda yaitu sinisme dan egoisme. Ini adalah drama zaman kita.
Itu adalah ateisme militan dan relativisme sinis, melalui upaya para penganutnya, yang menjerat kesadaran semua orang, tanpa kecuali, yang tertinggi. negarawan di Planet kita. Fetish antroposentrisme berkepala dua inilah yang melahirkan dan memperkenalkan ke dalam kesadaran jutaan orang apa yang disebut konsep ilmiah tentang “prinsip universal degradasi materi-energi”, yaitu. disintegrasi universal dari benda-benda yang muncul sebelumnya - tidak ada yang tahu caranya - di alam. Di tempat esensi fundamental absolut (lingkungan substansial universal), sebuah khayalan pseudo-ilmiah dari prinsip universal degradasi energi, dengan atribut mitosnya - "entropi", ditempatkan.
5. Sampah kontra sampah
Menurut gagasan tokoh-tokoh masa lalu seperti Leibniz, Newton, Torricelli, Lavoisier, Lomonosov, Ostrogradsky, Faraday, Maxwell, Mendeleev, Umov, J. Thomson, Kelvin, G. Hertz, Pirogov, Timiryazev, Pavlov, Bekhterev dan banyak lagi , banyak lainnya - Lingkungan dunia adalah esensi fundamental absolut (= substansi dunia = dunia eter = semua materi Alam Semesta = "intisari" Aristoteles), yang mengisi seluruh ruang dunia tak terbatas secara isotropis dan tanpa sisa dan merupakan Sumber dan Pembawa semua jenis energi di alam - “kekuatan gerak” yang tidak dapat dihancurkan, "kekuatan aksi".
Berbeda dengan ini, menurut pandangan dominan saat ini dalam sains dunia, “entropi” fiksi matematika dinyatakan sebagai esensi fundamental yang mutlak, dan juga beberapa “informasi”, yang baru-baru ini diumumkan oleh para tokoh akademis dunia, dengan sangat serius. -ditelepon. “Esensi fundamental universal”, tanpa bersusah payah memberikan definisi rinci pada istilah baru ini.
Menurut paradigma ilmiah yang pertama, keselarasan dan keteraturan kehidupan abadi Alam Semesta berkuasa di dunia, melalui pembaruan lokal yang terus-menerus (serangkaian kematian dan kelahiran) dari formasi material individu dalam skala yang berbeda.
Menurut paradigma pseudoscientific yang terakhir, dunia, yang pernah diciptakan dengan cara yang tidak dapat dipahami, sedang bergerak ke dalam jurang degradasi umum, pemerataan suhu menuju kematian umum dan universal di bawah kendali waspada dari superkomputer Dunia tertentu, yang memiliki dan membuang dari beberapa “informasi”.
Beberapa orang melihat di sekitar mereka kemenangan kehidupan kekal, sementara yang lain melihat di sekitar mereka pembusukan dan kematian, yang dikendalikan oleh Bank Informasi Dunia tertentu.
Perjuangan dua konsep pandangan dunia yang bertentangan secara diametris untuk mendominasi pikiran jutaan orang adalah titik sentral biografi umat manusia. Dan pertaruhan dalam perjuangan ini sangatlah besar.
Dan bukan suatu kebetulan bahwa sepanjang abad ke-20 lembaga ilmiah dunia sibuk memperkenalkan (yang dianggap sebagai satu-satunya teori energi bahan bakar yang mungkin dan menjanjikan). bahan peledak, racun dan obat-obatan sintetik, zat beracun, rekayasa genetika dengan kloning biorobot, dengan degenerasi umat manusia ke tingkat oligofrenia primitif, downs dan psikopat. Dan program serta rencana tersebut kini bahkan tidak disembunyikan dari publik.
Kebenaran dari kehidupan ini adalah: dunia yang paling makmur dan berkuasa dalam skala global aktivitas manusia diciptakan pada abad ke-20 oleh kata terakhir pemikiran ilmiah, baja: pornografi, narkoba, bisnis farmasi, perdagangan senjata, termasuk teknologi informasi dan psikotronik global. Bagian mereka dalam volume global seluruh aliran keuangan secara signifikan melebihi 50%.
Berikutnya. Setelah merusak alam di Bumi selama 1,5 abad, persaudaraan akademis dunia kini terburu-buru untuk “menjajah” dan “menaklukkan” ruang dekat Bumi, memiliki niat dan proyek ilmiah untuk mengubah ruang ini menjadi tempat pembuangan sampah untuk “kesenangan” mereka. teknologi. Tuan-tuan akademisi ini benar-benar penuh dengan gagasan setan yang didambakan untuk mengelola ruang sirkumsolar, dan bukan hanya di Bumi.
Dengan demikian, landasan paradigma persaudaraan akademis dunia para tukang batu bebas didasarkan pada landasan idealisme yang sangat subyektif (antroposentrisme), dan bangunan yang mereka sebut sebagai paradigma ilmiah bertumpu pada relativisme permanen dan sinis serta ateisme militan.
Namun laju kemajuan yang sebenarnya tidak dapat dielakkan. Dan, sama seperti semua kehidupan di Bumi menjangkau Matahari, demikian pula pikiran sebagian ilmuwan modern dan ilmuwan alam, tidak terbebani oleh kepentingan klan persaudaraan universal, menjangkau matahari Kehidupan abadi, gerakan abadi di Alam Semesta, melalui pengetahuan tentang kebenaran mendasar Keberadaan dan pencarian fungsi tujuan utama keberadaan dan evolusi spesies xomo sapiens. Sekarang, setelah mempertimbangkan sifat faktor psi, mari kita lihat Tabel Dmitry Ivanovich Mendeleev.
6. Argumentum ad rem
Apa yang kini disajikan di sekolah dan universitas dengan judul “Tabel Periodik Unsur Kimia D.I. Mendeleev” benar-benar palsu.
Terakhir kali Tabel Periodik yang sebenarnya diterbitkan dalam bentuk yang tidak terdistorsi adalah pada tahun 1906 di St. Petersburg (buku teks “Fundamentals of Chemistry”, edisi VIII).
Dan hanya setelah 96 tahun terlupakan, Tabel Periodik asli bangkit untuk pertama kalinya dari abu berkat publikasi disertasi ini di jurnal ZhRFM dari Masyarakat Fisik Rusia. Tabel D.I. Mendeleev “Tabel periodik unsur menurut golongan dan deret” (D. I. Mendeleev. Fundamentals of Chemistry. Edisi VIII, St. Petersburg, 1906)
Setelah kematian mendadak D.I. Mendeleev dan meninggalnya rekan-rekan ilmiahnya yang setia di Masyarakat Fisika-Kimia Rusia, untuk pertama kalinya ia mengangkat tangannya ke ciptaan abadi Mendeleev - putra dari teman dan koleganya D.I. Mendeleev di Masyarakat - Boris Nikolaevich Menshutkin. Tentu saja, Boris Nikolaevich juga tidak bertindak sendiri - dia hanya melaksanakan perintah. Bagaimanapun, paradigma baru relativisme menuntut penolakan terhadap gagasan tentang eter dunia; dan oleh karena itu persyaratan ini diangkat ke tingkat dogma, dan karya D.I. Mendeleev dipalsukan.
Distorsi utama Tabel adalah pengalihan “kelompok nol”. Tabelnya ada di akhir, di sebelah kanan, dan pendahuluan yang disebut. "periode". Kami menekankan bahwa manipulasi seperti itu (hanya pada pandangan pertama, tidak berbahaya) secara logis hanya dapat dijelaskan sebagai penghapusan secara sadar tautan metodologis utama dalam penemuan Mendeleev: sistem periodik unsur pada permulaannya, sumbernya, yaitu. di pojok kiri atas Tabel, harus ada grup nol dan baris nol, tempat elemen "X" berada (menurut Mendeleev - "Newtonium"), mis. siaran dunia.
Selain itu, sebagai satu-satunya unsur pembentuk sistem dari seluruh Tabel Unsur Turunan, unsur “X” ini adalah argumen dari keseluruhan Tabel Periodik. Pemindahan kelompok nol Tabel ke tujuannya menghancurkan gagasan tentang prinsip dasar seluruh sistem unsur menurut Mendeleev.
Untuk mengkonfirmasi hal di atas, kami akan memberikan penjelasan kepada D.I.
“...Jika analog argon tidak menghasilkan senyawa sama sekali, maka jelas bahwa tidak mungkin untuk memasukkan salah satu kelompok unsur yang diketahui sebelumnya, dan bagi mereka unsur tersebut harus dibuka. kelompok khusus nol... Posisi analog argon pada golongan nol ini merupakan konsekuensi logis dari pemahaman hukum periodik, dan oleh karena itu (penempatan pada golongan VIII jelas salah) diterima tidak hanya oleh saya, tetapi juga oleh Braizner, Piccini dan lainnya...
Sekarang, ketika sudah tidak diragukan lagi bahwa sebelum golongan I, di mana hidrogen harus ditempatkan, terdapat suatu golongan nol, yang wakil-wakilnya mempunyai berat atom lebih kecil daripada unsur-unsur golongan I, menurut saya mustahil untuk menyangkal keberadaan unsur yang lebih ringan dari hidrogen.
Dari jumlah tersebut, pertama-tama mari kita perhatikan elemen baris pertama kelompok pertama. Kami menyatakannya dengan “y”. Ia jelas memiliki sifat dasar gas argon... “Coronium”, dengan kepadatan sekitar 0,2 relatif terhadap hidrogen; dan itu tidak bisa menjadi eter dunia. Namun, elemen “y” ini diperlukan agar secara mental bisa mendekati elemen “x” yang paling penting dan paling cepat bergerak, yang menurut pemahaman saya, dapat dianggap sebagai eter. Saya ingin menyebutnya "Newtonium" - untuk menghormati Newton yang abadi... Masalah gravitasi dan masalah semua energi (!!!) tidak dapat dibayangkan akan benar-benar terpecahkan tanpa pemahaman nyata tentang eter sebagai media dunia yang mentransmisikan energi jarak jauh. Pemahaman yang sebenarnya tentang eter tidak dapat dicapai dengan mengabaikan sifat kimianya dan tidak menganggapnya sebagai zat dasar” (“An Attempt at a Chemical Understanding of the World Ether.” 1905, hal. 27).
“Unsur-unsur ini, berdasarkan besarnya berat atomnya, menempati tempat yang tepat di antara halida dan logam alkali, seperti yang ditunjukkan Ramsay pada tahun 1900. Dari unsur-unsur tersebut perlu dibentuk gugus nol khusus, yang pertama kali dikenali oleh Errere di Belgia pada tahun 1900. Saya menganggap berguna untuk menambahkan di sini bahwa, secara langsung dilihat dari ketidakmampuan untuk menggabungkan unsur-unsur golongan nol, analog argon harus ditempatkan lebih awal (!!!) daripada unsur-unsur golongan 1 dan, dalam semangat sistem periodik, mengharapkan a berat atomnya lebih rendah dibandingkan logam alkali.
Ternyata inilah yang terjadi. Dan jika demikian, maka keadaan ini, di satu sisi, berfungsi sebagai konfirmasi kebenaran prinsip periodik, dan di sisi lain, dengan jelas menunjukkan hubungan analog argon dengan unsur-unsur lain yang diketahui sebelumnya. Hasilnya, prinsip-prinsip yang dianalisis dapat diterapkan lebih luas daripada sebelumnya, dan mengharapkan unsur-unsur deret nol dengan berat atom jauh lebih rendah daripada hidrogen.
Jadi, dapat ditunjukkan bahwa pada baris pertama, pertama sebelum hidrogen, terdapat unsur golongan nol dengan berat atom 0,4 (mungkin ini koronium Yong), dan pada baris nol, pada golongan nol, ada adalah unsur pembatas dengan berat atom yang sangat kecil, tidak mampu melakukan interaksi kimia dan, sebagai akibatnya, memiliki pergerakan parsial (gas) yang sangat cepat.
Sifat-sifat ini, mungkin, harus dikaitkan dengan atom-atom dari dunia eter yang ada di mana-mana (!!!). Saya menunjukkan gagasan ini dalam kata pengantar publikasi ini dan dalam artikel jurnal Rusia tahun 1902…” (“Fundamentals of Chemistry.” Edisi VIII, 1906, hal. 613 et seq.).
7. Punctum garam
Berikut ini dengan jelas mengikuti kutipan-kutipan tersebut.
- Unsur-unsur golongan nol memulai setiap baris unsur-unsur lain, yang terletak di sisi kiri Tabel, "... yang merupakan konsekuensi logis dari pemahaman hukum periodik" - Mendeleev.
- Tempat yang sangat penting dan bahkan eksklusif dalam arti hukum periodik adalah milik elemen "x" - "Newtonium" - eter dunia. Dan elemen khusus ini harus ditempatkan di awal seluruh Tabel, dalam apa yang disebut “grup nol dari baris nol”. Selain itu, sebagai elemen pembentuk sistem (lebih tepatnya, esensi pembentuk sistem) dari semua elemen Tabel Periodik, eter dunia merupakan argumen penting bagi seluruh keragaman elemen Tabel Periodik. Tabel itu sendiri, dalam hal ini, bertindak sebagai fungsi tertutup dari argumen ini.
Sekarang mari kita beralih ke karya pemalsuan pertama Tabel Periodik.
8. Corpus delicti
Untuk menghapus dari kesadaran semua ilmuwan generasi berikutnya gagasan tentang peran eksklusif eter dunia (dan inilah yang dibutuhkan oleh paradigma relativisme baru), unsur-unsur kelompok nol secara khusus dipindahkan dari sisi kiri Tabel Periodik ke sisi kanan, memindahkan elemen yang sesuai satu baris lebih rendah dan menggabungkan grup nol dengan apa yang disebut. "kedelapan". Tentu saja, tidak ada tempat tersisa untuk elemen “y” atau elemen “x” dalam tabel yang dipalsukan.
Namun hal ini pun tidak cukup bagi persaudaraan relativis. Justru sebaliknya, pemikiran mendasar D.I. Mendeleev tentang peran penting eter dunia. Secara khusus, dalam kata pengantar Hukum Periodik versi pertama yang dipalsukan oleh D.I. Mendeleev, tanpa rasa malu, B.M. Menshutkin menyatakan bahwa Mendeleev diduga selalu menentang peran khusus eter dunia dalam proses alam. Berikut kutipan artikel B.N., yang sinismenya tak tertandingi. Menshutkina:
“Jadi (?!) kita kembali lagi ke pandangan itu, yang ditentang oleh (?!) selalu (?!!!) D. I. Mendeleev, yang sejak zaman paling kuno ada di kalangan para filsuf yang menganggap semua zat dan benda yang terlihat dan diketahui terdiri dari substansi utama yang sama dari para filsuf Yunani (“proteule” para filsuf Yunani, prima materia dari Romawi). Hipotesis ini selalu mendapat penganut karena kesederhanaannya dan dalam ajaran para filosof disebut hipotesis kesatuan materi atau hipotesis kesatuan materi." (B.N. Menshutkin. “D.I. Mendeleev. Periodic Law.” Diedit dan dengan artikel tentang situasi terkini hukum periodik oleh B.N. Menshutkin. State Publishing House, M-L., 1926).
9. Bersifat rerum
Menilai pandangan D.I. Mendeleev dan lawan-lawannya yang tidak bermoral, perlu diperhatikan hal-hal berikut.
Kemungkinan besar, Mendeleev tanpa disadari membuat kesalahan dalam fakta bahwa "eter dunia" adalah "zat dasar" (yaitu, "elemen kimia" - dalam pengertian modern). Kemungkinan besar, “eter dunia” adalah substansi yang sebenarnya; dan dengan demikian, dalam arti sempit, bukanlah suatu “substansi”; dan ia tidak memiliki “kimia dasar” yaitu. tidak memiliki “berat atom yang sangat rendah” dengan “gerakan parsial intrinsik yang sangat cepat”.
Biarkan D.I. Mendeleev salah dalam menilai “materialitas” dan “kimia” eter. Pada akhirnya, ini adalah kesalahan perhitungan terminologis seorang ilmuwan besar; dan pada masanya hal ini dapat dimaklumi, karena pada masa itu istilah-istilah tersebut masih cukup kabur, baru masuk dalam peredaran ilmiah. Tetapi ada hal lain yang sepenuhnya jelas: Dmitry Ivanovich benar sekali dalam hal bahwa "dunia eter" adalah esensi yang membentuk segalanya - intisari, substansi yang membentuk seluruh dunia benda (dunia material) dan di mana semua bentukan material tinggal. Dmitry Ivanovich juga benar bahwa zat ini mentransmisikan energi jarak jauh dan tidak memiliki aktivitas kimia apa pun. Keadaan terakhir hanya menegaskan gagasan kami bahwa D.I. Mendeleev sengaja memilih elemen “x” sebagai entitas yang luar biasa.
Jadi, "dunia eter", yaitu. substansi Alam Semesta bersifat isotropik, tidak memiliki struktur parsial, tetapi merupakan esensi mutlak (yaitu, hakikat tertinggi, fundamental, fundamental universal) dari Alam Semesta, Alam Semesta. Dan justru karena, sebagaimana dicatat dengan benar oleh D.I. Mendeleev, - eter dunia “tidak mampu melakukan interaksi kimia”, dan oleh karena itu bukan “elemen kimia”, yaitu. "substansi dasar" - dalam pengertian modern dari istilah-istilah ini.
Dmitry Ivanovich juga benar bahwa eter dunia adalah pembawa energi jarak jauh. Katakanlah lebih lanjut: eter dunia, sebagai substansi Dunia, tidak hanya sebagai pembawa, tetapi juga sebagai “penjaga” dan “pembawa” semua jenis energi (“kekuatan aksi”) di alam.
Sejak dahulu kala D.I. Mendeleev juga diamini oleh ilmuwan terkemuka lainnya, Torricelli (1608 - 1647): “Energi adalah intisari dari sifat yang begitu halus sehingga tidak dapat ditampung dalam wadah lain kecuali dalam substansi terdalam dari benda-benda material.”
Jadi menurut Mendeleev dan Torricelli siaran dunia adalah substansi terdalam dari benda-benda material. Itulah sebabnya “Newtonium” Mendeleev tidak hanya berada di baris nol dari golongan nol sistem periodiknya, tetapi ini adalah semacam “mahkota” dari seluruh tabel unsur kimianya. Mahkota, yang membentuk semua unsur kimia di dunia, yaitu. semuanya penting. Mahkota ini (“Ibu”, “Materi-Substansi” dari setiap zat) adalah Lingkungan alam, digerakkan dan didorong untuk berubah - menurut perhitungan kami - oleh entitas absolut (kedua) lainnya, yang kami sebut “Aliran substansial informasi fundamental primer tentang bentuk dan metode pergerakan Materi di Alam Semesta.” Rincian lebih lanjut mengenai hal ini dapat ditemukan di jurnal “Pemikiran Rusia”, 1-8, 1997, hlm.
Kami memilih “O”, nol, sebagai simbol matematika dari dunia eter, dan “rahim” sebagai simbol semantik. Pada gilirannya, kami memilih “1”, satu, sebagai simbol matematika dari Aliran Zat, dan “satu” sebagai simbol semantik. Jadi, berdasarkan simbolisme di atas, menjadi mungkin untuk diungkapkan secara ringkas dalam satu hal ekspresi matematika totalitas semua kemungkinan bentuk dan metode pergerakan materi di alam:
Ungkapan ini secara matematis mendefinisikan apa yang disebut. interval terbuka perpotongan dua himpunan - himpunan "O" dan himpunan "1", sedangkan definisi semantik dari ungkapan ini adalah "satu di dada" atau sebaliknya: Aliran substansial informasi fundamental primer tentang bentuk dan metode gerak Materi-substansi sepenuhnya meresapi substansi-Materi ini, yaitu. siaran dunia.
Dalam doktrin agama, “interval terbuka” ini dibalut dalam bentuk kiasan dari tindakan Universal penciptaan semua materi di Dunia oleh Tuhan dari Materi-Substansi, yang dengannya Dia terus-menerus berada dalam keadaan persetubuhan yang bermanfaat.
Penulis artikel ini sadar bahwa konstruksi matematika ini pernah diilhami olehnya, sekali lagi, meskipun kelihatannya aneh, oleh ide-ide D.I. Mendeleev, diungkapkan olehnya dalam karya-karyanya (lihat, misalnya, artikel “Upaya pemahaman kimiawi dunia eter”). Sekarang saatnya merangkum penelitian kita yang dituangkan dalam disertasi ini.
10. Kesalahan: ferro et igni
Pengabaian yang kategoris dan sinis oleh ilmu pengetahuan dunia terhadap tempat dan peran eter dunia dalam proses alam (dan dalam Tabel Periodik!) justru telah menimbulkan keseluruhan masalah bagi umat manusia di era teknokratis kita.
Salah satu permasalahan utama adalah bahan bakar dan energi.
Pengabaian peran eter dunia inilah yang memungkinkan para ilmuwan membuat kesimpulan yang salah (dan sekaligus licik) bahwa seseorang hanya dapat menghasilkan energi yang berguna untuk kebutuhan sehari-harinya dengan membakar, yaitu dengan membakar. menghancurkan zat (bahan bakar) secara permanen. Oleh karena itu muncullah tesis yang salah bahwa industri energi bahan bakar saat ini tidak mempunyai alternatif nyata. Dan jika demikian, maka, konon, hanya ada satu hal yang tersisa: menghasilkan energi nuklir (yang paling kotor secara ekologis!) dan produksi gas-minyak-batubara, membuang sampah sembarangan dan meracuni habitat kita sendiri.
Justru pengabaian peran eter dunialah yang mendorong semua ilmuwan nuklir modern untuk mencari “keselamatan” dengan cerdik melalui pembelahan atom dan partikel elementer dalam akselerator sinkrotron khusus yang mahal. Dalam eksperimen yang mengerikan dan sangat berbahaya ini, mereka ingin menemukan dan selanjutnya menggunakan apa yang disebut “demi kebaikan”. “plasma quark-gluon”, menurut gagasan salah mereka - seolah-olah “pra-materi” (istilah para ilmuwan nuklir itu sendiri), menurut teori kosmologis palsu mereka yang disebut. "Ledakan Besar Alam Semesta".
Patut dicatat, menurut perhitungan kami, jika ini disebut demikian. Jika “impian paling rahasia dari semua fisikawan nuklir modern” tercapai secara tidak sengaja, maka kemungkinan besar hal tersebut akan menjadi akhir dari semua kehidupan di bumi yang disebabkan oleh ulah manusia dan akhir dari planet bumi itu sendiri – benar-benar sebuah “Big Bang” dalam skala global, tapi bukan hanya untuk bersenang-senang, tapi nyata.
Oleh karena itu, eksperimen gila ilmu akademis dunia ini harus dihentikan secepat mungkin, yang terkena racun faktor psi dari ujung kepala sampai ujung kaki dan yang, tampaknya, bahkan tidak terbayangkan. konsekuensi bencana ide parascientific gila mereka.
D.I. Mendeleev ternyata benar: “Masalah gravitasi dan masalah semua energi tidak dapat dibayangkan dapat diselesaikan tanpa pemahaman nyata tentang eter sebagai media dunia yang mentransmisikan energi jarak jauh.”
D.I. Mendeleev juga benar dalam hal bahwa “suatu hari nanti mereka akan menyadari bahwa mempercayakan urusan industri tertentu kepada orang-orang yang tinggal di dalamnya tidak akan membawa hasil terbaik, meskipun mendengarkan orang-orang seperti itu berguna.”
“Makna pokok dari apa yang telah dikatakan adalah bahwa kepentingan-kepentingan yang bersifat umum, abadi dan abadi seringkali tidak sejalan dengan kepentingan pribadi dan sementara, bahkan sering bertentangan satu sama lain, dan menurut saya sebaiknya diutamakan jika tidak memungkinkan lagi. untuk mendamaikan - yang pertama daripada yang kedua. Ini adalah drama zaman kita.” D.I.Mendeleev. “Pemikiran untuk pengetahuan Rusia.” 1906
Jadi, eter dunia adalah substansi dari setiap unsur kimia dan, oleh karena itu, dari setiap substansi, ia merupakan materi sejati Absolut sebagai Esensi pembentuk unsur Semesta.
Eter dunia adalah sumber dan mahkota seluruh Tabel Periodik asli, awal dan akhir - alfa dan omega dari Tabel Periodik Unsur Dmitry Ivanovich Mendeleev.
Bagaimana cara menggunakan tabel periodik? Bagi orang yang belum tahu, membaca tabel periodik sama dengan bagi gnome yang melihat rune kuno para elf. Dan tabel periodik, jika digunakan dengan benar, dapat memberi tahu banyak hal tentang dunia. Selain membantu Anda dengan baik dalam ujian, ini juga tidak tergantikan dalam memecahkan sejumlah besar masalah kimia dan fisika. Tapi bagaimana cara membacanya? Untungnya, saat ini semua orang dapat mempelajari seni ini. Pada artikel ini kami akan memberi tahu Anda cara memahami tabel periodik.
Tabel periodik unsur kimia (tabel Mendeleev) adalah klasifikasi unsur kimia yang menetapkan ketergantungan berbagai sifat unsur pada muatan inti atom.
Sejarah Penciptaan Tabel
Dmitry Ivanovich Mendeleev bukanlah seorang ahli kimia sederhana, jika ada yang berpikir demikian. Dia adalah seorang ahli kimia, fisikawan, ahli geologi, ahli metrologi, ahli ekologi, ekonom, pekerja minyak, aeronaut, pembuat instrumen dan guru. Semasa hidupnya, ilmuwan tersebut berhasil banyak melakukan penelitian mendasar di berbagai bidang ilmu pengetahuan. Misalnya, diyakini secara luas bahwa Mendeleev-lah yang menghitung kekuatan ideal vodka - 40 derajat. Kami tidak tahu bagaimana perasaan Mendeleev tentang vodka, tetapi kami tahu pasti bahwa disertasinya dengan topik “Wacana tentang kombinasi alkohol dengan air” tidak ada hubungannya dengan vodka dan mempertimbangkan konsentrasi alkohol dari 70 derajat. Dengan segala kelebihan ilmuwan, penemuan hukum periodik unsur kimia - salah satu hukum dasar alam, memberinya ketenaran terluas.

Ada legenda yang menyatakan bahwa seorang ilmuwan memimpikan tabel periodik, setelah itu yang harus dia lakukan hanyalah menyempurnakan gagasan yang muncul. Tapi, jika semuanya sesederhana itu.. Versi pembuatan tabel periodik ini, rupanya, tidak lebih dari sebuah legenda. Ketika ditanya bagaimana meja dibuka, Dmitry Ivanovich sendiri menjawab: “ Saya sudah memikirkannya mungkin selama dua puluh tahun, tetapi Anda berpikir: Saya sedang duduk di sana dan tiba-tiba... selesai.”
Pada pertengahan abad kesembilan belas, upaya untuk menyusun unsur-unsur kimia yang diketahui (63 unsur diketahui) dilakukan secara paralel oleh beberapa ilmuwan. Misalnya, pada tahun 1862, Alexandre Emile Chancourtois menempatkan unsur-unsur di sepanjang heliks dan mencatat pengulangan siklik sifat kimia. Ahli kimia dan musisi John Alexander Newlands mengusulkan tabel periodik versinya pada tahun 1866. Fakta menarik adalah ilmuwan tersebut mencoba menemukan semacam harmoni musik mistis dalam susunan unsur-unsurnya. Di antara upaya lainnya, ada juga upaya Mendeleev yang berhasil.

Pada tahun 1869, diagram tabel pertama diterbitkan, dan tanggal 1 Maret 1869 dianggap sebagai hari dibukanya hukum periodik. Inti dari penemuan Mendeleev adalah bahwa sifat-sifat unsur dengan bertambahnya massa atom tidak berubah secara monoton, melainkan secara berkala. Tabel versi pertama hanya berisi 63 elemen, namun Mendeleev melakukan sejumlah elemen solusi non-standar. Jadi, dia menebak untuk menyisakan ruang di tabel untuk unsur-unsur yang masih belum ditemukan, dan juga mengubah massa atom beberapa unsur. Kebenaran mendasar dari hukum yang diturunkan oleh Mendeleev dikonfirmasi segera, setelah ditemukannya galium, skandium dan germanium, yang keberadaannya telah diprediksi oleh ilmuwan tersebut.
Pandangan modern tentang tabel periodik
Di bawah ini adalah tabelnya sendiri

Saat ini, alih-alih berat atom (massa atom), konsep nomor atom (jumlah proton dalam inti) digunakan untuk mengurutkan unsur-unsur. Tabel tersebut berisi 120 unsur, yang disusun dari kiri ke kanan berdasarkan kenaikan nomor atom (jumlah proton)
Kolom tabel mewakili apa yang disebut kelompok, dan baris mewakili periode. Tabel ini memiliki 18 grup dan 8 periode.
- Sifat logam suatu unsur berkurang bila bergerak sepanjang periode dari kiri ke kanan, dan bertambah dalam arah sebaliknya.
- Ukuran atom mengecil ketika bergerak dari kiri ke kanan sepanjang periode.
- Saat Anda berpindah dari atas ke bawah melalui golongan, sifat logam pereduksi meningkat.
- Sifat pengoksidasi dan non-logam meningkat ketika bergerak sepanjang periode dari kiri ke kanan SAYA.
Apa yang kita pelajari tentang suatu elemen dari tabel? Misalnya, mari kita ambil elemen ketiga dalam tabel - litium, dan pertimbangkan secara mendetail.

Pertama-tama, kita melihat simbol elemen itu sendiri dan namanya di bawahnya. Di pojok kiri atas terdapat nomor atom suatu unsur, urutan unsur tersebut disusun dalam tabel. Nomor atom, sebagaimana telah disebutkan, sama dengan jumlah proton dalam inti atom. Jumlah proton positif biasanya sama dengan jumlah elektron negatif dalam suatu atom (kecuali isotop).
Massa atom ditunjukkan di bawah nomor atom (dalam tabel versi ini). Jika kita membulatkan massa atom ke bilangan bulat terdekat, kita mendapatkan apa yang disebut nomor massa. Perbedaan antara nomor massa dan nomor atom menunjukkan jumlah neutron dalam inti atom. Jadi, jumlah neutron dalam inti helium adalah dua, dan dalam litium adalah empat.
Kursus kami “Tabel Periodik untuk Boneka” telah berakhir. Sebagai penutup, kami mengundang Anda untuk menonton video tematiknya, dan kami berharap pertanyaan tentang cara menggunakan tabel periodik Mendeleev menjadi lebih jelas bagi Anda. Kami mengingatkan Anda bahwa mempelajari mata pelajaran baru selalu lebih efektif tidak sendirian, tetapi dengan bantuan mentor yang berpengalaman. Itu sebabnya Anda tidak boleh melupakan mereka, yang dengan senang hati akan berbagi pengetahuan dan pengalamannya dengan Anda.
instruksi
Sistem periodik adalah “rumah” bertingkat yang berisi banyak apartemen. Setiap “penyewa” atau di apartemennya sendiri dengan nomor tertentu, yang bersifat permanen. Selain itu, unsur tersebut memiliki “nama belakang” atau nama, seperti oksigen, boron, atau nitrogen. Selain data ini, setiap “apartemen” berisi informasi seperti massa atom relatif, yang mungkin memiliki nilai pasti atau bulat.
Seperti halnya rumah mana pun, ada “pintu masuknya”, yaitu berkelompok. Apalagi secara berkelompok unsur-unsurnya terletak di kiri dan kanan, membentuk. Tergantung pada sisi mana yang lebih banyak, sisi itu disebut sisi utama. Oleh karena itu, subgrup lainnya akan menjadi subgrup sekunder. Tabel juga memiliki “lantai” atau titik. Selain itu, titik dapat berukuran besar (terdiri dari dua baris) dan kecil (hanya memiliki satu baris).
Tabel tersebut menunjukkan struktur atom suatu unsur, yang masing-masing memiliki inti bermuatan positif yang terdiri dari proton dan neutron, serta elektron bermuatan negatif yang berputar mengelilinginya. Jumlah proton dan elektron secara numerik sama dan ditentukan dalam tabel berdasarkan nomor urut unsur. Misalnya unsur kimia belerang #16, maka ia mempunyai 16 proton dan 16 elektron.
Untuk menentukan jumlah neutron (partikel netral juga terletak di dalam inti), kurangi nomor atomnya dari massa atom relatif suatu unsur. Misalnya besi mempunyai massa atom relatif 56 dan nomor atom 26. Oleh karena itu, 56 – 26 = 30 proton untuk besi.
Elektron terletak pada jarak yang berbeda dari inti, membentuk tingkat elektron. Untuk menentukan jumlah tingkat elektronik (atau energi), Anda perlu melihat jumlah periode di mana unsur tersebut berada. Misal di periode ke 3, maka dari itu akan ada 3 level.
Berdasarkan nomor golongan (tetapi hanya untuk subgrup utama), valensi tertinggi dapat ditentukan. Misalnya, unsur-unsur golongan pertama dari subkelompok utama (litium, natrium, kalium, dll.) memiliki valensi 1. Oleh karena itu, unsur-unsur golongan kedua (berilium, kalsium, dll.) akan memiliki valensi 2.
Anda juga dapat menganalisis properti elemen menggunakan tabel. Dari kiri ke kanan, logam, dan non-logam diperkuat. Hal ini terlihat jelas pada contoh periode 2: dimulai dengan logam alkali, kemudian logam alkali tanah magnesium, setelah itu unsur aluminium, kemudian silikon nonlogam, fosfor, belerang dan periode diakhiri dengan zat gas - klor dan argon. Pada periode berikutnya, ketergantungan serupa diamati.
Dari atas ke bawah, sebuah pola juga diamati - sifat logam meningkat, dan sifat non-logam melemah. Misalnya, cesium jauh lebih aktif dibandingkan natrium.
Untuk kenyamanan, lebih baik menggunakan versi warna tabel.
Penemuan hukum periodik dan penciptaan sistem keteraturan unsur kimia D.I. Mendeleev menjadi puncak perkembangan ilmu kimia pada abad ke-19. Ilmuwan merangkum dan mensistematisasikan pengetahuan luas tentang sifat-sifat unsur.
instruksi
Pada abad ke-19 belum ada gagasan tentang struktur atom. Penemuan oleh D.I. Mendeleev hanyalah generalisasi fakta eksperimental, tetapi makna fisiknya masih belum jelas untuk waktu yang lama. Ketika data pertama tentang struktur inti dan distribusi elektron dalam atom muncul, hukum dan sistem unsur dapat dilihat dengan cara baru. Tabel D.I. Mendeleev memungkinkan untuk menelusuri secara visual sifat-sifat unsur yang ditemukan di dalamnya.
Setiap elemen dalam tabel diberi nomor seri tertentu (H - 1, Li - 2, Be - 3, dst). Angka ini sesuai dengan inti (jumlah proton dalam inti) dan jumlah elektron yang mengorbit inti. Dengan demikian, jumlah proton sama dengan jumlah elektron, yang berarti bahwa dalam kondisi normal atom bersifat elektrik.
Pembagian menjadi tujuh periode terjadi sesuai dengan jumlah tingkat energi atom. Atom-atom periode pertama memiliki kulit elektron satu tingkat, periode kedua memiliki kulit elektron dua tingkat, periode ketiga memiliki kulit elektron tiga tingkat, dan seterusnya. Ketika tingkat energi baru terisi, periode baru dimulai.
Unsur pertama pada periode mana pun dicirikan oleh atom yang memiliki satu elektron di tingkat terluar - ini adalah atom logam alkali. Periode berakhir dengan atom gas mulia, yang memiliki tingkat energi eksternal terisi penuh dengan elektron: pada periode pertama, gas mulia memiliki 2 elektron, pada periode berikutnya - 8. Justru karena kesamaan struktur kulit elektron itulah kelompok unsur mempunyai sifat fisika yang serupa.
Di tabel D.I. Mendeleev memiliki 8 subgrup utama. Jumlah ini ditentukan oleh jumlah maksimum elektron pada tingkat energi.
Di bagian bawah tabel periodik, lantanida dan aktinida dibedakan sebagai deret independen.
Menggunakan tabel D.I. Mendeleev, seseorang dapat mengamati periodisitas sifat-sifat unsur berikut: jari-jari atom, volume atom; potensi ionisasi; kekuatan afinitas elektron; keelektronegatifan atom; ; sifat fisik senyawa potensial.
Periodisitas susunan unsur-unsur dalam tabel D.I. Mendeleev dijelaskan secara rasional oleh sifat berurutan dari pengisian tingkat energi dengan elektron.
Sumber:
- Tabel periodik
Hukum periodik yang menjadi dasar ilmu kimia modern dan menjelaskan pola perubahan sifat-sifat unsur kimia ditemukan oleh D.I. Mendeleev pada tahun 1869. Makna fisik dari hukum ini terungkap dengan mempelajari struktur kompleks atom.

Pada abad ke-19 diyakini bahwa massa atom adalah karakteristik utama unsur, sehingga digunakan untuk mengklasifikasikan zat. Saat ini, atom ditentukan dan diidentifikasi berdasarkan jumlah muatan pada intinya (nomor dan nomor atom pada tabel periodik). Namun, massa atom suatu unsur, dengan beberapa pengecualian (misalnya, massa atom lebih kecil dari massa atom argon), meningkat sebanding dengan muatan inti unsur tersebut.
Dengan bertambahnya massa atom, terjadi perubahan periodik pada sifat-sifat unsur dan senyawanya. Ini adalah sifat logam dan non-logam atom, jari-jari atom, potensial ionisasi, afinitas elektron, keelektronegatifan, bilangan oksidasi, senyawa (titik didih, titik leleh, massa jenis), kebasaan, amfoterisitas atau keasaman.
Berapa banyak unsur yang ada dalam tabel periodik modern
Tabel periodik secara grafis mengungkapkan hukum yang ditemukannya. Tabel periodik modern mengandung 112 unsur kimia (yang terakhir adalah Meitnerium, Darmstadtium, Roentgenium dan Copernicium). Menurut data terakhir, 8 unsur berikut juga telah ditemukan (hingga 120 inklusif), namun tidak semuanya mendapat namanya, dan unsur-unsur tersebut masih sedikit di publikasi cetak mana pun.
Setiap unsur menempati sel tertentu dalam tabel periodik dan memiliki nomor seri sendiri-sendiri, sesuai dengan muatan inti atomnya.
Bagaimana tabel periodik dibuat?
Struktur tabel periodik diwakili oleh tujuh periode, sepuluh baris dan delapan golongan. Setiap periode dimulai dengan logam alkali dan diakhiri dengan gas mulia. Pengecualiannya adalah periode pertama, yang dimulai dengan hidrogen, dan periode ketujuh yang tidak lengkap.
Periode dibagi menjadi kecil dan besar. Periode kecil (pertama, kedua, ketiga) terdiri dari satu baris horizontal, periode besar (keempat, kelima, keenam) terdiri dari dua baris horizontal. Baris atas dalam periode besar disebut genap, baris bawah disebut ganjil.
Pada periode keenam tabel setelah (nomor urut 57) terdapat 14 unsur yang sifatnya mirip dengan lantanum - lantanida. Mereka tercantum di bagian bawah tabel sebagai baris terpisah. Hal yang sama berlaku untuk aktinida yang terletak setelah aktinium (dengan nomor 89) dan sebagian besar mengulangi sifat-sifatnya.
Barisan genap periode besar (4, 6, 8, 10) hanya diisi dengan logam.
Unsur-unsur dalam golongan menunjukkan valensi yang sama dalam oksida dan senyawa lain, dan valensi ini sesuai dengan nomor golongannya. Yang utama mengandung unsur periode kecil dan besar, hanya yang besar. Dari atas ke bawah menguat, nonlogam melemah. Semua atom subkelompok samping adalah logam.
Tip 4: Selenium sebagai unsur kimia pada tabel periodik
Unsur kimia selenium termasuk golongan VI tabel periodik Mendeleev, merupakan kalkogen. Selenium alami terdiri dari enam isotop stabil. Ada juga 16 isotop radioaktif selenium yang diketahui.

instruksi
Selenium dianggap sebagai elemen yang sangat langka dan sangat langka; ia bermigrasi dengan cepat di biosfer, membentuk lebih dari 50 mineral. Yang paling terkenal adalah: berzelianite, naumannite, selenium asli dan chalcomenite.
Selenium ditemukan dalam belerang vulkanik, galena, pirit, bismutin dan sulfida lainnya. Itu ditambang dari timah, tembaga, nikel dan bijih lainnya, yang ditemukan dalam keadaan tersebar.
Jaringan sebagian besar makhluk hidup mengandung 0,001 hingga 1 mg/kg, beberapa tanaman, organisme laut dan jamur memusatkannya. Untuk sejumlah tanaman, selenium merupakan elemen penting. Kebutuhan manusia dan hewan adalah 50-100 mcg/kg makanan; unsur ini memiliki sifat antioksidan, mempengaruhi banyak reaksi enzimatik dan meningkatkan sensitivitas retina terhadap cahaya.
Selenium dapat ada dalam berbagai modifikasi alotropik: amorf (selenium kaca, bubuk dan koloidal), serta kristal. Dengan mereduksi selenium dari larutan asam selenosa atau dengan mendinginkan uapnya dengan cepat, diperoleh bubuk merah dan selenium koloidal.
Ketika modifikasi unsur kimia ini dipanaskan di atas 220°C dan kemudian didinginkan, selenium kaca akan terbentuk;
Yang paling stabil secara termal adalah selenium abu-abu heksagonal, yang kisi-kisinya dibangun dari rantai spiral atom yang terletak sejajar satu sama lain. Ini diproduksi dengan memanaskan bentuk selenium lain hingga meleleh dan perlahan mendingin hingga 180-210°C. Dalam rantai selenium heksagonal, atom-atomnya terikat secara kovalen.
Selenium stabil di udara, tidak terpengaruh oleh: oksigen, air, sulfur encer dan asam klorida, namun, ia larut dengan baik dalam asam nitrat. Berinteraksi dengan logam, selenium membentuk selenida. Ada banyak senyawa kompleks selenium yang diketahui, semuanya beracun.
Selenium diperoleh dari kertas atau limbah produksi dengan pemurnian tembaga secara elektrolitik. Unsur ini terdapat dalam lumpur bersama dengan logam berat, belerang dan telurium. Untuk mengekstraknya, lumpur disaring, kemudian dipanaskan dengan asam sulfat pekat atau dipanggang oksidatif pada suhu 700°C.
Selenium digunakan dalam produksi penyearah dioda semikonduktor dan peralatan konverter lainnya. Dalam metalurgi, digunakan untuk memberi baja struktur berbutir halus dan juga meningkatkan sifat mekaniknya. Dalam industri kimia, selenium digunakan sebagai katalis.
Sumber:
- KhiMiK.ru, Selen
Kalsium adalah suatu unsur kimia yang termasuk dalam subkelompok kedua tabel periodik dengan simbol Ca dan massa atom 40,078 g/mol. Ini adalah logam alkali tanah yang cukup lunak dan reaktif dengan warna keperakan.

instruksi
DENGAN bahasa Latin“” diterjemahkan sebagai “kapur” atau “batu lunak”, dan penemuannya berasal dari orang Inggris Humphry Davy, yang pada tahun 1808 mampu mengisolasi kalsium menggunakan metode elektrolitik. Ilmuwan kemudian mengambil campuran jeruk nipis basah, “dibumbui” dengan merkuri oksida, dan melakukan proses elektrolisis pada pelat platinum, yang muncul dalam percobaan sebagai anoda. Katoda adalah kawat yang dicelupkan oleh ahli kimia ke dalam cairan merkuri. Menarik juga bahwa senyawa kalsium seperti batu kapur, marmer dan gipsum, serta kapur, telah dikenal umat manusia berabad-abad sebelum eksperimen Davy, di mana para ilmuwan percaya bahwa beberapa di antaranya adalah benda yang sederhana dan mandiri. Baru pada tahun 1789 Lavoisier dari Prancis menerbitkan sebuah karya yang menyatakan bahwa kapur, silika, barit, dan alumina adalah zat kompleks.
Kalsium punya derajat tinggi aktivitas kimia, sehingga praktis tidak ditemukan di alam dalam bentuk murni. Namun para ilmuwan memperkirakan bahwa unsur ini menyumbang sekitar 3,38% dari total massa seluruh kerak bumi, menjadikan kalsium paling melimpah kelima setelah oksigen, silikon, aluminium, dan besi. Ada elemen ini di dalamnya air laut– sekitar 400 mg per liter. Kalsium juga termasuk dalam berbagai silikat batu(misalnya granit dan gneisses). Banyak terdapat pada feldspar, kapur dan batugamping, terdiri dari mineral kalsit dengan rumus CaCO3. Bentuk kristal kalsium adalah marmer. Totalnya, melalui migrasi unsur ini di kerak bumi, terbentuk 385 mineral.
KE sifat fisik Kalsium mengacu pada kemampuannya untuk menunjukkan kemampuan semikonduktor yang berharga, meskipun ia tidak menjadi semikonduktor dan logam dalam pengertian tradisional. Situasi ini berubah dengan peningkatan tekanan secara bertahap, ketika kalsium diberi keadaan logam dan kemampuan untuk menunjukkan sifat superkonduktor. Kalsium mudah berinteraksi dengan oksigen, kelembaban udara dan karbon dioksida, karena unsur kimia ini disimpan rapat-rapat di laboratorium untuk bekerja dan ahli kimia John Alexander Newland - namun, komunitas ilmiah mengabaikan pencapaiannya. Usulan Newland tidak dianggap serius karena pencariannya akan harmoni dan hubungan antara musik dan chemistry.
Dmitri Mendeleev pertama kali menerbitkan tabel periodiknya pada tahun 1869 di halaman Journal of Russian Chemical Society. Ilmuwan tersebut juga mengirimkan pemberitahuan tentang penemuannya kepada semua ahli kimia terkemuka dunia, setelah itu dia berulang kali memperbaiki dan menyempurnakan tabel tersebut hingga menjadi seperti yang dikenal sekarang. Inti dari penemuan Dmitry Mendeleev adalah perubahan sifat kimia unsur secara periodik, bukan monoton seiring dengan bertambahnya massa atom. Penyatuan terakhir teori tersebut ke dalam hukum periodik terjadi pada tahun 1871.
Legenda tentang Mendeleev
Legenda yang paling umum adalah ditemukannya tabel periodik dalam mimpi. Ilmuwan itu sendiri telah berulang kali mengejek mitos ini, mengklaim bahwa dia telah menemukan tabel tersebut selama bertahun-tahun. Menurut legenda lain, vodka Dmitry Mendeleev - muncul setelah ilmuwan mempertahankan disertasinya "Wacana tentang kombinasi alkohol dengan air".
Mendeleev masih dianggap oleh banyak orang sebagai penemunya, yang suka berkreasi dengan larutan air-alkohol. Ilmuwan sezamannya sering menertawakan laboratorium Mendeleev, yang ia dirikan di lubang pohon ek raksasa.
Alasan terpisah untuk bercanda, menurut rumor, adalah hasrat Dmitry Mendeleev untuk menenun koper, yang dilakukan ilmuwan tersebut saat tinggal di Simferopol. Belakangan, ia membuat kerajinan tangan dari karton untuk kebutuhan laboratoriumnya, sehingga ia secara sinis disebut ahli pembuatan koper.
Tabel periodik, selain mengurutkan unsur-unsur kimia ke dalam satu sistem, juga memungkinkan untuk memprediksi penemuan banyak unsur baru. Namun, pada saat yang sama, para ilmuwan mengakui beberapa di antaranya tidak ada, karena tidak sesuai dengan konsep tersebut. Paling sejarah yang diketahui pada saat itu terjadi penemuan unsur-unsur baru seperti koronium dan nebulium.