ज्वलन हवेचा वापर आणि इंधन ज्वलन उत्पादनांचे प्रमाण. इंधन ज्वलन दरम्यान रासायनिक प्रतिक्रिया
भट्टीमध्ये ज्वलन प्रक्रियेचे मुख्य गुणात्मक वैशिष्ट्य म्हणजे त्याची रासायनिक पूर्णता कमीत कमी जास्त हवेसह, जी उच्चतम दहन तापमानाशी संबंधित आहे. म्हणून, ज्वलन प्रक्रिया आयोजित करताना, दहन उत्पादनांच्या रचनेचे पद्धतशीरपणे निरीक्षण करणे आणि जास्त हवेचे गुणांक आणि ज्वलनाची रासायनिक अपूर्णता निर्धारित करणे आवश्यक आहे. या उद्देशासाठी, गॅस विश्लेषण वापरले जाते, विविध प्रणालींचे गॅस विश्लेषक वापरून केले जाते आणि मूलभूत दहन समीकरणावर आधारित गणना पद्धतीवर आधारित आहे.
पूर्ण ज्वलनाच्या समीकरणाचा विचार करूया. दहन उत्पादनांमधील ऑक्सिजनच्या संतुलनावर आधारित या समीकरणाची व्युत्पत्ती डी.एम. खझमल्यान [एल. 4].
पूर्ण ज्वलनाच्या वेळी, ऑक्सिडायझर म्हणून पुरवलेल्या हवेत असलेला ऑक्सिजन कार्बन, सल्फर आणि कार्बन डायऑक्साइडच्या निर्मितीसह इंधनाच्या मुक्त हायड्रोजनच्या ज्वलनासाठी वापरला जातो, सल्फर डायऑक्साइड, पाण्याची वाफ, आणि जास्तीचा भाग मुक्त स्वरूपात राहतो, म्हणजे:
K. =0.2"/. = C + C + C, O + ^o,- (2-42)
सूत्रात:
Uv आणि U®a - 1 किलो इंधन जाळण्यासाठी पुरविलेल्या हवेचे प्रमाण आणि त्यात असलेल्या ऑक्सिजनचे प्रमाण, m3/kg;
C. Ud*0 - अनुक्रमे, कार्बन डायऑक्साइड, सल्फर डायऑक्साइड तयार करण्यासाठी आणि 1 किलो इंधन, m*/kg च्या ज्वलनाच्या वेळी मुक्त हायड्रोजनच्या ज्वलनासाठी ऑक्सिजनचा वापर;
U0a म्हणजे मुक्त ऑक्सिजनचे प्रमाण, m3/kg.
स्टोइचियोमेट्रिक समीकरणे (2-1) आणि (2-2) नुसार, इंधनाच्या संपूर्ण ज्वलनासह, कार्बनच्या ज्वलनासाठी ऑक्सिजनचा वापर कार्बन डायऑक्साइडच्या प्रमाणात तयार होतो आणि सल्फरच्या ज्वलनासाठी ऑक्सिजनचा वापर होतो. तयार झालेल्या सल्फर डायऑक्साइडच्या आकारमानाच्या बरोबरीने, म्हणजे.
Ус°2 = V У50* - V
IOA уСОа» коа
म्हणून, कार्बन आणि सल्फर इंधनाच्या ज्वलनासाठी ऑक्सिजनचा वापर समान आहे
C+C^ae. + "^^o,- (2-43)
(2-43) बदलून आम्ही समीकरण (2-42) फॉर्ममध्ये बदलतो:
K. = 0.21V, = V + V™ + V (2-42a)
हवेतील नायट्रोजन दहन उत्पादनांमध्ये जाते. त्याची रक्कम सैद्धांतिक आणि नायट्रोजन V°Ma च्या अतिरिक्त प्रमाणाच्या बेरजेने निर्धारित केली जाते आणि
Y£°, घन आणि कमी सामग्रीमुळे इंधनातून गॅसिफाइड नायट्रोजनच्या प्रमाणाकडे दुर्लक्ष करणे द्रव इंधन(कमी
1.5-1.8%). मुक्त ऑक्सिजन V0a सह अतिरिक्त नायट्रोजन
जास्त हवेचे प्रतिनिधित्व करते (a-1)U°. ऑक्सिजन आणि नायट्रोजनच्या दिलेल्या घटकांच्या एकूण हवेच्या प्रवाहाची तुलना सूत्रानुसार (2-12) कोरड्या वायूंच्या प्रमाणाशी केल्यास, आम्ही निष्कर्षापर्यंत पोहोचतो की
^ = आम्हाला. g + Uo;°- (2-44)
(2-44) समीकरण (2-42a) मध्ये बदलल्यानंतर आम्हाला मिळते:
समीकरण (2-45) मध्ये समाविष्ट असलेल्या सर्व अटी कोरड्या वायूंच्या प्रमाणाच्या टक्केवारीच्या रूपात व्यक्त केल्याने आणि ते सुलभ केल्याने आम्हाला मिळते:
21 = 1?02 + 02 + 79 . (2-46)
ट्रायॲटॉमिक वायूंच्या व्हॉल्यूमद्वारे कोरड्या वायूंचे प्रमाण व्यक्त करणे Vc. g = = आम्ही समीकरण (2-46) तथाकथित समीकरणाच्या स्वरूपात पुन्हा लिहितो
पूर्ण ज्वलन परिस्थिती:
21 = IOg + Og + pIOg, ($2-47
ज्यामध्ये p सूचित करतो
T/NaO T/NaO
(2-48) समीकरणानुसार (2-3) 1^*° चे मूल्य बदलून, हे गृहीत धरून की हायड्रोजनचा भाग इंधन ऑक्सिजनमुळे ऑक्सिडाइझ झाला आहे आणि (2-7) नुसार मूल्य, अभिव्यक्ती p साठी इंधनाच्या मूलभूत रचनेद्वारे फॉर्ममध्ये दर्शविले जाऊ शकते:
पी = 2.35<2-48а?
गुणांक p (2-48) चा भौतिक अर्थ असा आहे की ते मुक्त इंधन हायड्रोजनच्या ऑक्सिडेशनसाठी हवेच्या ऑक्सिजनच्या वापराचे प्रमाण दर्शविते (म्हणजे इंधन हायड्रोजन, त्याचा इंधन ऑक्सिजनशी संबंधित भाग वगळून) 0.01 (क्रमांक -0.126 किंवा) ट्रायटोमिक वायूंच्या निर्मितीसाठी ऑक्सिजनच्या वापरासाठी.
दहन उत्पादनांमधील O2 ची ज्ञात टक्केवारी आणि गुणांक p च्या आधारावर, समीकरण (2-47) वापरून, ट्रायटोमिक वायूंची टक्केवारी निश्चित करणे शक्य आहे:
02-0 वर, म्हणजे a-1 वर, I02 सामग्री त्याच्या कमाल मूल्यापर्यंत पोहोचते
VD “a”: = t|t. "(2-50!
जर इंधनाचे ज्वलनशील घटक कार्बन आणि सल्फर असतील आणि त्यात ऑक्सिजन आणि हायड्रोजन नसेल किंवा इंधनाच्या ऑक्सिजनमुळे त्याचे ऑक्सिडीकरण होऊ शकेल इतके हायड्रोजन असेल, तर इंधनाचे संपूर्ण ज्वलन झाल्यावर हवेची सैद्धांतिकदृष्ट्या आवश्यक मात्रा, ट्रायॲटॉमिक वायूंची सामग्री 21% असेल, जसे की या प्रकरणात (2-50) (2-48a) p = 0 नुसार.
हायड्रोजनच्या संपूर्ण ऑक्सिडेशनसाठी आवश्यक असलेल्या घन आणि द्रव इंधनांमध्ये सामान्यतः कमी ऑक्सिजन असते; म्हणून, ज्वलनाच्या वेळी, हवेतील ऑक्सिजनचा काही भाग इंधनाच्या मुक्त हायड्रोजन 0.01 (Hp-0.126 0p) च्या ऑक्सिडेशनसाठी वापरला जातो. म्हणून, कोरड्या वायूंमध्ये I02 सामग्री 21% पेक्षा कमी असेल आणि (2-49) द्वारे निर्धारित केली जाऊ शकते.
अभिव्यक्ती (2-48a) आणि (2-49) वरून पाहिल्याप्रमाणे, गुणांक p आणि IOg चे मूल्य केवळ इंधनाच्या प्राथमिक रासायनिक रचनेवर अवलंबून असते आणि म्हणूनच ते इंधनाची महत्त्वपूर्ण वैशिष्ट्ये आहेत. काही इंधनांसाठी P आणि I02max ची मूल्ये तक्त्यामध्ये दिली आहेत. 2-3.
|
गुणांक (3 आणि काही इंधनांसाठी मूल्य 102aKS
|
ज्वलनशील इंधन पदार्थ हवेच्या ऑक्सिजनशी विशिष्ट परिमाणात्मक प्रमाणात संवाद साधतात. ज्वलनासाठी हवेचा वापर आणि इंधन ज्वलन उत्पादनांचे प्रमाण स्टोइचियोमेट्रिक दहन समीकरणे वापरून मोजले जाते, जे प्रत्येक दहनशील घटकासाठी 1 किमीसाठी लिहिलेले असते.
सैद्धांतिक आणि वास्तविक दहन हवा वापर आणि इंधन ज्वलन उत्पादनांचे प्रमाण. घन आणि द्रव इंधनाच्या ज्वलनशील घटकांच्या ज्वलनासाठी स्टोचिओमेट्रिक समीकरणे खालीलप्रमाणे आहेत:
कार्बन C + O 2 = CO 2:
12 kg C + 32 kg O 2 = 44 kG CO 2;
1 किलो C + (32:12) kg O 2 = (44:12) kg CO 2 (18.21)
सल्फर S + O 2 = SO 2:
32 kg S + 32 kg O 2 = 64 kg SO 2;
1 किलो S + 1 kg O 2 = 2 kg SO 2; (18.22)
हायड्रोजन 2H 2 + O 2 = 2H 2 O:
4 kg H 2 + 32 kg O 2 = 36 kg H 2 O;
1 kg H 2 + 8 kg O 2 = 9 kg H 2 (18.23)
इंधनामध्ये C p/100 kg कार्बन, S p/l 100 kg अस्थिर सल्फर, H p/100 kg हायड्रोजन आणि O p/100 kg ऑक्सिजन असते. परिणामी, स्टोइचियोमेट्रिक समीकरणांनुसार, 1 किलो इंधनाच्या ज्वलनासाठी आवश्यक असलेला ऑक्सिजनचा एकूण वापर, समान असेल:
हवेतील ऑक्सिजनचे वस्तुमान अंश 0.232 आहे. मग हवेचे वस्तुमान प्रमाण सूत्रानुसार निर्धारित केले जाते:

सामान्य परिस्थितीत, हवेची घनता p0 = 1.293 kg/m3.
ज्वलन हवेचा वापर आणि इंधन ज्वलन उत्पादनांचे प्रमाण याप्रमाणे सहज मोजले जाऊ शकते:
V 0 = M 0 /1.293 m 3 हवा/किलो इंधन (18.26)
अशा प्रकारे,
V 0 = 0.0889 (C p + 0.375S p / l) + 0.265H p - 0.033O p (18.27)
वायू इंधनासाठी, वापर V0 स्टोइचिओमेट्रिक प्रतिक्रिया वापरून गॅसमध्ये समाविष्ट केलेल्या दहनशील घटकांच्या व्हॉल्यूम अंशांवर आधारित निर्धारित केला जातो:
H 2 + 0.5O 2 = H 2 O;
CO + 0.5O 2 = CO 2;
CH 4 + 2O 2 = CO 2 + 2H 2 O;
H 2 S + 1.5 O 2 = SO 2 + H 2 O. (18.28)
वायूच्या ज्वलनासाठी आवश्यक असलेल्या हवेचे सैद्धांतिक प्रमाण, m 3 / m 3, सूत्राद्वारे निर्धारित केले जाते:
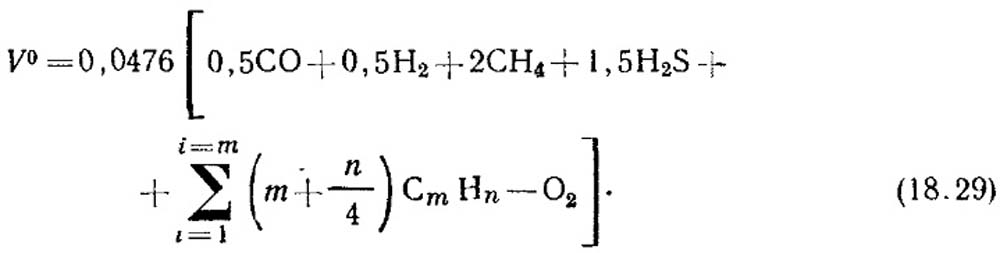
घटकांची घनता एकाग्रता, %, समीकरणात बदलली जाते (18.29). असंतृप्त हायड्रोकार्बन्सच्या एकाग्रतेबद्दल कोणताही डेटा नसल्यास, त्यांना C 2 H 4 मानले जाते.
स्टोइचियोमेट्रिक समीकरणे (18.27) आणि (18.29) वापरून मोजले जाणारे हवेचे V n चे प्रमाण सैद्धांतिकदृष्ट्या आवश्यक असे म्हटले जाते, म्हणजे V 0 हे मूल्य 1 किलो (1 मीटर 3) चे पूर्ण ज्वलन सुनिश्चित करण्यासाठी आवश्यक हवेचे किमान प्रमाण आहे. इंधन, जर त्यातील सर्व ऑक्सिजन आणि इंधनामध्ये असलेला ऑक्सिजन ज्वलन दरम्यान वापरला जाईल.
भट्टीच्या कार्यरत व्हॉल्यूममध्ये हवेसह इंधन पूर्ण मिसळण्याची प्रक्रिया आयोजित करण्यात काही अडचणींमुळे, स्थानिक कमतरता किंवा ऑक्सिडायझरची जास्ती जाणवेल अशी क्षेत्रे दिसू शकतात. परिणामी, दहन हवेची गुणवत्ता आणि वापर आणि इंधन ज्वलन उत्पादनांचे प्रमाण बिघडते. म्हणून, वास्तविक परिस्थितीत, इंधन ज्वलनासाठी हवा त्याच्या सैद्धांतिक प्रमाण V 0 च्या तुलनेत मोठ्या प्रमाणात पुरवली जाते. सैद्धांतिकदृष्ट्या आवश्यक असलेल्या फायरबॉक्सला पुरवलेल्या हवेच्या वास्तविक प्रमाणाच्या गुणोत्तराला अतिरिक्त वायु गुणांक म्हणतात:
α = V d /V 0.(18.30)
भट्टी किंवा इतर दहन कक्षांची रचना आणि थर्मली गणना करताना, जळलेल्या इंधनाचा प्रकार, ज्वलन पद्धत आणि दहन कक्षांच्या डिझाइन वैशिष्ट्यांवर अवलंबून a चे मूल्य निवडले जाते. मूल्य 1.02 ते 1.5 पर्यंत असते.
इंधनाच्या संपूर्ण ज्वलनाच्या उत्पादनांची रचना आणि प्रमाण. α = 1 वर इंधनाच्या संपूर्ण ज्वलनाच्या उत्पादनांमध्ये हे समाविष्ट आहे: कोरडे (बॉयलर युनिटमध्ये नॉन-कंडेन्सिंग) ट्रायटॉमिक वायू CO 2 आणि SO 2;
H 2 O - हायड्रोजनच्या ज्वलनातून मिळणारी पाण्याची वाफ; एन 2 - हवेच्या सैद्धांतिकदृष्ट्या आवश्यक प्रमाणात असलेले इंधन नायट्रोजन आणि नायट्रोजन.
याव्यतिरिक्त, ज्वलन उत्पादनांमध्ये इंधनाच्या आर्द्रतेच्या बाष्पीभवनामुळे निर्माण होणारी पाण्याची वाफ, ओलसर हवेसह भट्टीत वाफ आणली जाते आणि कधीकधी अणूकरणासाठी इंधन तेल जळताना वापरली जाणारी वाफ यांचा समावेश होतो. जेव्हा दहन उत्पादनांचे तापमान दवबिंदू तापमानापेक्षा कमी असते तेव्हा पाण्याची वाफ घनरूप होते. α = 1 सह पूर्ण ज्वलनासह, दहन उत्पादनांमध्ये फक्त CO 2, SO 2, H 2 O आणि N 2 असेल; जर α > 1 असेल, तर त्यामध्ये अतिरिक्त हवा देखील असेल, म्हणजे ऑक्सिजन आणि नायट्रोजनची अतिरिक्त मात्रा.
खंडानुसार संबंधित वायूंची टक्केवारी CO 2, N 2, SO 2, इ. आणि V co2, V so2, V n2, इ. द्वारे दर्शविली जाईल. - 1 किलो (1 एम 3) इंधन जाळून मिळवलेले त्यांचे खंड, सामान्य स्थितीत कमी केले जातात (निर्देशांक 0 दर्शवते की गणना α = 1 वर केली जाते). मग आम्हाला मिळते:
CO 2 + SO 2 + N 0 / 2 + H 2 O 2 = 100%
V 0 / r = V co2 + V S2O + V 0 / N2 + V 0 H2O (18.31)
जेथे V o / r हे ज्वलन उत्पादनांचे एकूण प्रमाण आहे, सामान्य स्थितीत कमी केले जाते, m 3 / kg.
गणिते सोपी करण्यासाठी, कोरड्या ट्रायटॉमिक वायूंचे परिमाण एकत्रितपणे मोजले जातात आणि त्यांची बेरीज पारंपारिकपणे RO 2 चिन्हाद्वारे नियुक्त केली जाते, म्हणजे.
V ro2 = V co2 + V so2 (18.32)
समानतेतील पहिल्या तीन घटकांची बेरीज (18.31) कोरड्या वायूंचे प्रमाण V с.p दर्शवते आणि म्हणून,
V o r = V o c.g + V 0 H2O (18.33)
जेथे V 0 c.r = V ro2 + V 0 N2
V 0 N2, V 0 H2O, V 0 c.r, V 0 आणि V ro2 हे 1 किलो घन किंवा द्रव इंधन जळताना (18.21) आणि (18.22) च्या वस्तुमानानुसार वायूंचे सैद्धांतिक खंड आहेत ट्रायटोमिक वायू समान आहेत:
कार्बन डाय ऑक्साईड आणि सल्फर डायऑक्साइडची घनता, सामान्य स्थितीत कमी केली जाते, अनुक्रमे p co2 = 1.964 kg/m 3 आणि P so2 = 2.86 kg/m 3 च्या समान आहेत. मग ट्रायटॉमिक वायू V RO2 चे प्रमाण सूत्राद्वारे निर्धारित केले जाऊ शकते:

हायड्रोजन V r H2O च्या ज्वलनाच्या वेळी तयार झालेल्या पाण्याच्या वाफेचे सैद्धांतिक परिमाण समीकरण (18.23) नुसार निर्धारित केले जाते. या व्हॉल्यूममध्ये इंधन ओलावा V r H2O च्या बाष्पीभवनादरम्यान तयार झालेल्या वाफेचे प्रमाण जोडणे आवश्यक आहे. नोजल स्टीम V f H2O ची मात्रा आणि H2O मधील हवेत V मध्ये असलेल्या पाण्याच्या वाफेचे प्रमाण नंतर: 
जेथे 0.805 ही सामान्य भौतिक परिस्थितीत पाण्याच्या वाफेची घनता आहे, kg/m 3 ; W f - नोजल वाफेचा वापर (ग्राह्य W f = 0.3 ÷ 0.35 kg/kg),
पाण्याच्या वाफेची एकूण सैद्धांतिक मात्रा सूत्राद्वारे निर्धारित केली जाते:
V 0 H 2 O = 0.111H p + 0.0124 W p + 1.24 W f + 0.0161 V 0 (18.41)
α = 1 वर नायट्रोजनचे सैद्धांतिक खंड (1 m3 प्रति 1 किलो इंधन) मध्ये हवा नायट्रोजन आणि इंधन नायट्रोजन असते, म्हणजे.
जेथे p N2 = 1.25 - नायट्रोजन घनता, kg/m 3.
जेव्हा अतिरीक्त हवेचे गुणांक α > 1 असेल तेव्हा ज्वलन उत्पादनांच्या रचनेत या हवेसह अतिरिक्त हवा आणि पाण्याची वाफ समाविष्ट असेल. येथे ज्वलन उत्पादनांचे खंड
α = 1 ला वास्तविक खंड म्हणतात.
वास्तविक खंड असतील:
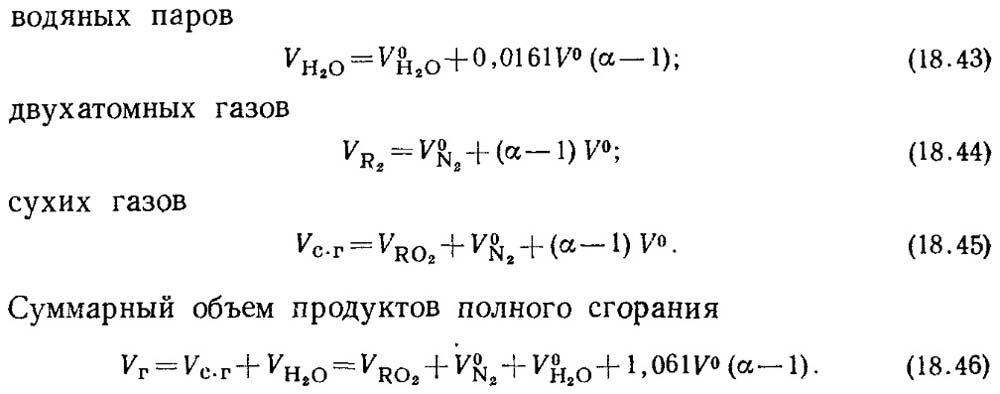
V RO2 चे मूल्य अतिरिक्त वायु गुणांकाच्या मूल्यावर अवलंबून नाही.
वायू इंधनाच्या 1 मीटर 3 च्या ज्वलन उत्पादनांच्या सैद्धांतिक खंडांची गणना स्टॉइचियोमेट्रिक प्रतिक्रियांच्या आधारे केली जाते (18.28). वायू इंधन CO, H 2 आणि C m H n च्या ज्वलनशील घटकांच्या संपूर्ण ज्वलनाने, कार्बन डायऑक्साइड CO 2 आणि पाण्याची वाफ तयार होते. जेव्हा हायड्रोजन सल्फाइड H 2 S जाळला जातो तेव्हा पाण्याच्या वाफ व्यतिरिक्त, सल्फर डायऑक्साइड SO 2 तयार होतो.
ट्रायटॉमिक वायूंचे प्रमाण, m 3 / m 3,

जेथे a आहे गॅसची आर्द्रता सामग्री, g/m3.
नायट्रोजन, कोरड्या वायूंचे प्रमाण आणि ज्वलन उत्पादनांची एकूण मात्रा तसेच द्रव आणि घन इंधनांसाठी (18.42), (18.33) आणि (18.31) सूत्रे वापरून निर्धारित केले जातात.
α > 1 साठी, (18.43), (18.45) आणि (18.46) सूत्रे वापरून पाण्याची वाफ, कोरडा वायू आणि ज्वलन उत्पादनांचे एकूण प्रमाण आढळते. जर गॅसमध्ये समाविष्ट असलेल्या असंतृप्त हायड्रोकार्बन्स CnH2n ची रचना अज्ञात असेल आणि त्यांची एकूण सामग्री 3% पेक्षा जास्त नसेल, तर गणनामध्ये ते C2H4 म्हणून विचारात घेतले जातात.
गॅस विश्लेषण परिणामांवर आधारित दहन गणना. ज्वलन उत्पादनांचे गॅस विश्लेषण हे इंधन ज्वलनाची गुणवत्ता (पूर्णता) नियंत्रित करण्यासाठी आहे. या उद्देशासाठी, रासायनिक वायू विश्लेषक जसे की व्हीटीआय आणि जीपीसी - 3 वापरले जातात त्यांच्या ऑपरेशनचे सिद्धांत रासायनिक अभिकर्मकांद्वारे दहन उत्पादनांमध्ये समाविष्ट असलेल्या घटकांच्या निवडक शोषणावर आधारित आहे जे गॅस विश्लेषकांचे शोषण स्तंभ भरतात. उदाहरणार्थ, RO 2 शोषण्यासाठी एक KOH द्रावण वापरले जाते आणि O 2 शोषण्यासाठी pyrogallol C 6 H 3 (OH) 3 चे अल्कधर्मी द्रावण वापरले जाते.
सध्या, क्रोमॅटोग्राफिक गॅस विश्लेषणाचा मोठ्या प्रमाणावर वापर केला जातो, गॅस मिश्रणांना त्यांच्या घटक घटकांमध्ये वेगळे करण्यासाठी भौतिक पद्धतींवर आधारित. क्रोमॅटोग्राफच्या ऑपरेशनचे सिद्धांत विविध वायूंच्या शोषण गुणधर्मांमधील फरकावर आधारित आहे कारण ते सॉर्बेंट (सिलिका जेल) च्या थरातून जातात.
कोरड्या वायूंच्या व्हॉल्यूमसाठी गॅस विश्लेषणाच्या परिणामांवर आधारित गणना केली जाते.
घन आणि द्रव इंधनाच्या ज्वलनाच्या वेळी कार्बन मोनोऑक्साइडचे निर्धारण. जेव्हा इंधन अपूर्णपणे जाळले जाते, तेव्हा ज्वलन उत्पादनांमध्ये नेहमी काही प्रमाणात कार्बन मोनोऑक्साइड CO असते. कोरड्या ज्वलन उत्पादनांच्या रचनेचे समीकरण फॉर्म आहे
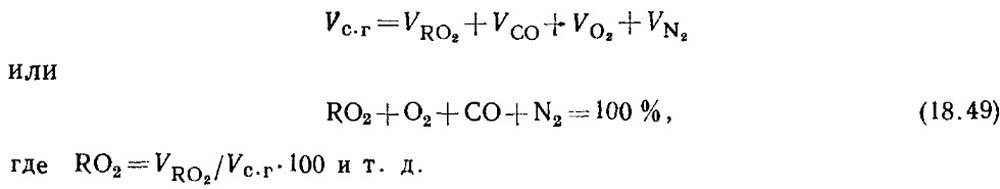
गॅस विश्लेषणाच्या परिणामांवर आधारित, दहन उत्पादनांमध्ये आरओ 2 आणि ओ 2 ची टक्केवारी निश्चित केली जाते.
शोषण पद्धतीचा वापर करून CO चे निर्धारण या पद्धतीच्या मोठ्या त्रुटीमुळे अवांछित आहे. म्हणून, वायूंमधील CO सामग्री गणनाद्वारे निर्धारित केली जाते.
शुद्ध कार्बन आणि α = 1 च्या पूर्ण ज्वलनासह, दहन उत्पादनांमध्ये CO 2 आणि N 2 असतो, COmax2 = RO max2 = 21% सह. कार्बन व्यतिरिक्त, जीवाश्म इंधनाच्या ज्वलनशील वस्तुमानात नेहमी काही प्रमाणात हायड्रोजन असते. म्हणून, कोरड्या ज्वलन उत्पादनांमध्ये RO मॅक्स 2 चे प्रमाण नेहमीच 21% पेक्षा कमी असते, म्हणजेच इंधनातील कार्बन आणि सल्फरचे प्रमाण कमी झाल्याने, RO max 2 चे मूल्य देखील कमी होते. कोरड्या ज्वलन उत्पादनांमध्ये इंधनाची मूलभूत रचना आणि तीन अणू वायूंची सामग्री यांच्यातील संबंध प्रस्थापित करण्यासाठी एक विशिष्ट परिमाणहीन प्रमाण आहे. या मूल्याला इंधन वैशिष्ट्य म्हणतात, आणि β अक्षराने दर्शविले जाते.
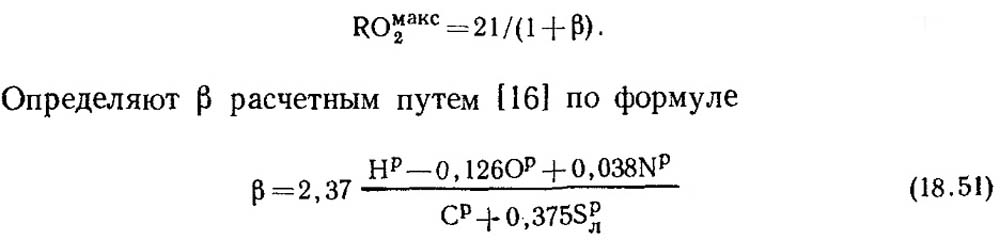
विशिष्ट रचनांच्या प्रत्येक प्रकारच्या इंधनासाठी RO कमाल 2 आणि β ची मूल्ये स्थिर असतात (तक्ता 18.4).
तक्ता 18.4. काही इंधनांसाठी RO कमाल 2 आणि β मूल्ये.
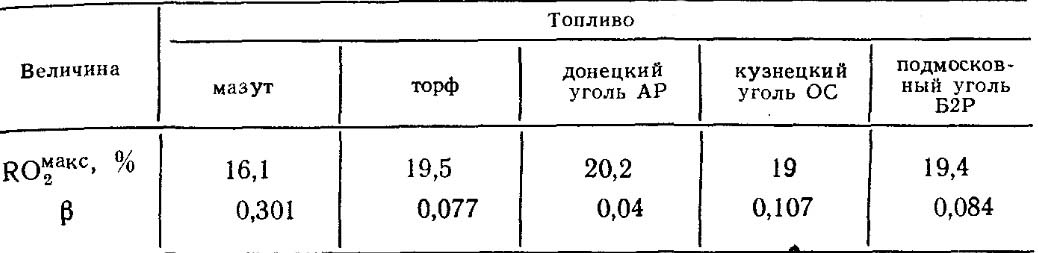
जसजसे अतिरिक्त हवेचे गुणांक β एकतेच्या वर वाढते, तसतसे अतिरिक्त हवेच्या परिणामी संपूर्ण ज्वलनाच्या कोरड्या उत्पादनांमध्ये मुक्त ऑक्सिजन आणि RO 2 दिसून येतील.< RO мак с 2 . При известном значении α содержание RО 2 можно приближенно определять по эмпирической формуле:
RO 2 = RO कमाल 2 / α (18.52)
विशेष साहित्यात, इंधनाच्या संपूर्ण ज्वलनासाठी तथाकथित समीकरण प्राप्त केले आहे:
RO 2 + O 2 = 21 β RO 2. (18.53)
जर समीकरणाच्या उजव्या आणि डाव्या बाजू (18.53) एकमेकांच्या समान नसतील, तर पूर्ण ज्वलन होत नाही आणि या प्रकरणात फरक (21 - βPRO 2 l) - (RO 2 + O 2) = z म्हणतात. इंधनाच्या अपूर्ण ज्वलनाचे वैशिष्ट्य.
इंधनाच्या अपूर्ण ज्वलनाचे समीकरण खालीलप्रमाणे लिहिले आहे:
21 - β RO 2 = RO 2 + O 2 + (0.605 + β) CO.(18.53")
गॅस विश्लेषणाची क्रोमॅटोग्राफिक पद्धत वापरताना, फॉर्म्युला (18.54) वापरून CO ची गणना करण्याची आवश्यकता नाही, कारण कार्बन मोनोऑक्साइड सामग्री थेट क्रोमॅटोग्राफवर निर्धारित केली जाऊ शकते.
ज्वलनासाठी हवेचा वापर आणि अपूर्ण दहन दरम्यान इंधन दहन उत्पादनांचे प्रमाण. खालीलप्रमाणे समीकरण (18.49) नुसार गॅस विश्लेषणाच्या परिणामांवरून कोरड्या ज्वलन उत्पादनांची मात्रा निर्धारित केली जाते. वायूंमध्ये आरओ 2 ची टक्केवारी:

वायू इंधनाच्या अपूर्ण दहन दरम्यान ज्वलनशील CO घटक CO, CH 4 आणि H 2 चे निर्धारण. कोरड्या ज्वलन उत्पादनांसाठी रचना समीकरण खालीलप्रमाणे लिहिले जाऊ शकते:
गॅस विश्लेषणाच्या क्रोमॅटोग्राफिक पद्धतीचा वापर करून, दहन उत्पादनांच्या CO, CH 4 आणि H 2 च्या ज्वलनशील भागाचे सर्व घटक निर्धारित करणे शक्य आहे.
जर विश्लेषणाचे परिणाम केवळ RO 2 आणि O 2 साठी ज्ञात असतील, तर वायूंमध्ये CO निश्चित करण्यासाठी, इंधन वैशिष्ट्यपूर्ण β चे मूल्य संदर्भ डेटावरून घेतले जाते किंवा, प्रारंभिक दहनशील वायूची रचना ज्ञात असल्यास, β आहे. गॅसमधील CO t 2 सामग्रीचा अनिवार्य विचार करून गणना करून निर्धारित केले जाते:

हे लक्षात घ्यावे की कृत्रिम वायूंसाठी ज्यामध्ये मोठ्या प्रमाणात CO t 2 असते, इंधन वैशिष्ट्य β नकारात्मक असू शकते.
अतिरिक्त हवा गुणांक निश्चित करणे. अतिरिक्त हवा गुणांक कोरड्या ज्वलन उत्पादनांच्या गॅस विश्लेषण डेटावरून निर्धारित केले जाते. पूर्ण ज्वलनाच्या बाबतीत, ज्वलन उत्पादनांमध्ये CO, CH 4, H 2 असे कोणतेही ज्वलनशील घटक नसतात.
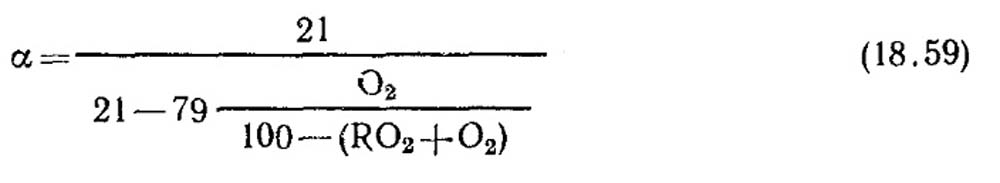
अपूर्ण दहन बाबतीत
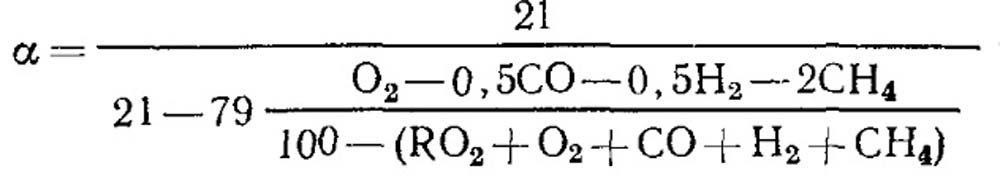
इंधनाच्या संपूर्ण ज्वलनासह आणि RO कमाल 2 चे ज्ञात मूल्य, सूत्र (18.52) निर्धारित करण्यासाठी वापरले जाऊ शकते.
उदाहरण. खालील व्हॉल्यूमेट्रिक रचना असलेल्या नैसर्गिक सेराटोव्ह (एल्शान) वायूच्या ज्वलनाची कमी आणि उच्च उष्णता निश्चित करा,%: CH 4 - 94, C 2 H 6 - 1.8, C 3 H 8 - 0.4, C 4 H 10 - 0, 1 , C 5 H 12 - 0.1,
CO 2 - 0.1, N 2 - 3.5.
उपाय: 1. सर्वात कमी उष्मांक मूल्य, kJ/m 3, आहे: मिथेन CH 4 - 35.8 × 10 3, इथेन C 2 H 4 - 64.6 × 10 3, प्रोपेन C 3 H 8 - 91.5 × 10 3, ब्युटेन C 4 H 10 - 119.0 × 10 3, pentane C 5 H 12 - 146.5 × 10 3.
सूत्र (18.6) वापरून आम्ही निर्धारित करतो
Q c n = (35.8×94 + 64.6×1.8 + 91.5×0.4+ 119×0.1 + 146.5×0.1) 103×0.01 = 35,300 kJ/m 3.
सर्वोच्च उष्मांक मूल्य, kJ/m 3, आहे: मिथेन CH 4 - 39.8 × 10 3, इथेन C 2 H 4 - 70 × 10 3, प्रोपेन C 3 H 8 - 99.5 × 10 3, ब्युटेन C 4 H 10 - 28.5 × 10 3, पेंटेन सी 8 एच 12 - 157.5 × 10 3.
सूत्र (18.17) वापरून आपण शोधतो
Q с в = (39.8 × 94 + 70 × 1.8 + 99.5 × 0.4 + 128.5 × 0.1 +157.5 × 0.01) 103 × 0.01 = 39,300 kJ/m 3.
इंजिन सिलेंडरमध्ये इंधन ज्वलन ही एक जटिल रासायनिक प्रक्रिया आहे. ज्वलन प्रक्रियेचे सर्व मध्यवर्ती टप्पे वगळून, आम्ही हवेतील ऑक्सिजनसह इंधन तयार करणाऱ्या घटकांच्या अंतिम रासायनिक अभिक्रियांचा विचार करू.
द्रव इंधनाच्या संपूर्ण दहन दरम्यान रासायनिक प्रतिक्रिया. इंधनाची मूलभूत रचना समीकरण (36) द्वारे निर्धारित केली जाते.
इंधनाच्या संपूर्ण ज्वलनासह, असे गृहीत धरले जाते की वातावरणातील ऑक्सिजनसह कार्बन आणि हायड्रोजनच्या प्रतिक्रियांच्या परिणामी, अनुक्रमे कार्बन डायऑक्साइड आणि पाण्याची वाफ तयार होतात. या प्रकरणात, इंधनाचे कार्बन आणि हायड्रोजनचे ऑक्सीकरण रासायनिक समीकरणांशी संबंधित आहे:
वस्तुमान एककांमध्ये प्रारंभिक आणि अंतिम प्रतिक्रिया उत्पादनांची गणना करताना, आम्ही प्राप्त करतो: C kg I C I साठी

kmol मध्ये गणना केल्यावर

समीकरणे (40) आणि (41) वरून हे स्पष्ट आहे की ऑक्सिजनसह कार्बनच्या प्रतिक्रियेच्या परिणामी, CO2 प्रतिक्रियेच्या अंतिम उत्पादनांच्या मोल्सची मात्रा प्रतिक्रियेत सहभागी होणाऱ्या ऑक्सिजनच्या व्हॉल्यूमच्या समान असते. ऑक्सिजनसह हायड्रोजनच्या अभिक्रियांमुळे वापरल्या जाणाऱ्या ऑक्सिजनच्या तुलनेत पाण्याच्या वाफेचे प्रमाण (मोलची संख्या) दुप्पट वाढते.
द्रव इंधनाच्या संपूर्ण दहन दरम्यान हवेच्या सैद्धांतिकदृष्ट्या आवश्यक प्रमाणाचे निर्धारण. ऑक्सिजन O0 ची सर्वात कमी मात्रा ज्याला त्याच्या संपूर्ण ऑक्सिडेशनसाठी बाहेरून इंधनाचा पुरवठा करावा लागतो त्याला सैद्धांतिकदृष्ट्या आवश्यक प्रमाणात ऑक्सिजन म्हणतात. समीकरण (38) आणि (39) वरून असे दिसून येते की 1 किलो इंधनाच्या संपूर्ण ज्वलनासाठी, गणना करताना खालील प्रमाणात ऑक्सिजन आवश्यक आहे:
![]()
किंवा kmol मध्ये गणना करताना (40) आणि (41) समीकरणांनुसार
![]()
अंतर्गत ज्वलन इंजिनमध्ये, ज्वलनासाठी आवश्यक ऑक्सिजन हवेमध्ये असतो, जो सेवन प्रक्रियेदरम्यान सिलेंडरमध्ये प्रवेश केला जातो. हवेतील ऑक्सिजनमध्ये वस्तुमानानुसार अंदाजे 23% आणि व्हॉल्यूमनुसार 21% असते, हे लक्षात घेता, आम्हाला ज्वलनासाठी सैद्धांतिकदृष्ट्या आवश्यक हवेची मात्रा मिळते.
किलोमध्ये 1 किलो इंधन:
![]()
किंवा kmol मध्ये
![]()
म्हणून:
![]()
ज्वलनासाठी स्टोचिओमेट्रिक मिश्रणाची रचना इंधन वैशिष्ट्य 6 द्वारे शोधली जाऊ शकते, जी सूत्राद्वारे निर्धारित केली जाते
वायुमंडलीय हवेमध्ये ज्वलनाच्या वेळी इंधन p" ची वैशिष्ट्ये इंधनाची मूलभूत रचना आणि हवेतील ऑक्सिजनचे प्रमाण यावर अवलंबून असतात.
काही परिवर्तनांनंतर, गणना करताना सूत्र (45).
![]()
(kmol मध्ये) फॉर्म घेईल
टेबलमध्ये दिले आहेत. ५.
" moles 02, आणि परिणामी m/z moles I20 तयार होतो. नंतर, दिलेल्या वायूमध्ये ऑक्सिजन O2 चे अस्तित्व लक्षात घेऊन, घटकाची ऑक्सीकरण प्रतिक्रिया समीकरणाद्वारे व्यक्त केली जाते.

फॉर्म्युलावर आधारित ऑक्सिजनसह (49) फॉर्म आहे
अभिव्यक्तीवरून निश्चित केले जाईल
वायू इंधनातील वैयक्तिक घटकांचे खंड अपूर्णांक.
जादा हवा गुणांक. कार इंजिनमध्ये, मिश्रण तयार करण्याच्या प्रकारावर, इंधनाच्या प्रज्वलन आणि ज्वलनाची परिस्थिती आणि ऑपरेटिंग मोडवर अवलंबून, वास्तविकपणे वापरल्या जाणाऱ्या हवेचे प्रमाण संपूर्ण दहनासाठी सैद्धांतिकदृष्ट्या आवश्यक त्यापेक्षा जास्त, समान किंवा कमी असू शकते.
kmol मध्ये) 1 किलो इंधनाच्या ज्वलनासाठी सैद्धांतिकदृष्ट्या आवश्यक असलेल्या हवेच्या प्रमाणास अतिरिक्त वायु गुणांक म्हणतात आणि खालील द्वारे दर्शविला जातो:
![]()
(अतिरिक्त ऑक्सिजन), मिश्रणाला दुबळे म्हणतात.
ऑक्सिजनच्या कमतरतेमुळे
डिझेल इंजिनमध्ये ज्यामध्ये उच्च-गुणवत्तेचे नियमन वापरले जाते, गुणांक a लोडच्या आधारावर मोठ्या प्रमाणात बदलतो (कमी लोडवर 5 किंवा अधिक ते पूर्ण लोडवर 1.41.25 पर्यंत). अंजीर मध्ये. आकृती 18 इंजिन लोडवर गुणांक a चे अवलंबित्व दर्शविते.
xg चा वापर अनेकदा इंजिन ऑपरेटिंग प्रक्रियेच्या विश्लेषणामध्ये केला जातो आणि त्याला हवा-इंधन प्रमाण म्हणतात.
(पूर्ण ज्वलन). स्पार्क इग्निशन इंजिनमध्ये, सेवन प्रक्रियेदरम्यान हवा आणि इंधन सिलेंडरमध्ये ज्वलनशील मिश्रण म्हणून प्रवेश करतात. 1 किलो इंधनाच्या संपूर्ण ज्वलनासह, एकूण दहनशील मिश्रणाचे प्रमाण (kmol मध्ये), ज्यामध्ये इंधनाची वाफ आणि हवा असते,
![]()
जेथे rt हे इंधनाचे आण्विक वजन आहे (तक्ता 5 पहा).
डिझेल इंजिनमध्ये, कॉम्प्रेशन प्रक्रियेच्या शेवटी आणि ज्वलन प्रक्रियेदरम्यान इंधन इंजेक्शन दरम्यान दहन चेंबरमध्ये हवा-इंधन मिश्रण तयार होते. याचा परिणाम म्हणून, आणि व्यापलेल्या लहान व्हॉल्यूममुळे, इंधनाचे आण्विक वस्तुमान विचारात घेतले जात नाही,
वायू इंधनासाठी (kmol किंवा m3 मध्ये)
कोणत्याही इंधनासाठी, मिश्रण वस्तुमान (किलोमध्ये)
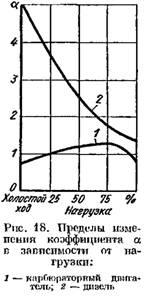
ज्वलन उत्पादनांच्या वैयक्तिक घटकांचे प्रमाण (kmol मध्ये) खालील समीकरणांद्वारे निर्धारित केले जाते:

प्रतिक्रियेत भाग घेणारे ऑक्सिजनचे वस्तुमान, kmol.
आम्हाला मिळते (kmol मध्ये)
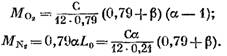
अभिव्यक्ती (58), (60) आणि (62) ला समीकरण (57) मध्ये बदलल्यानंतर, आम्हाला आढळते:
त्याचे मूल्य अभिव्यक्ती (45), आपल्याकडे असेल (kmol मध्ये)
इंधनाच्या वैशिष्ट्यांद्वारे दहन उत्पादनांचे प्रमाण (kmol मध्ये) निश्चित करूया. (58), (59), (61) आणि (62) सूत्रांमधून आपल्याकडे आहे
योग्य परिवर्तनानंतर आपल्याला मिळते
![]()
![]()
ज्वलन उत्पादनांचे प्रमाण (kmol मध्ये)
त्यानुसार, ज्वलन उत्पादनांमध्ये अतिरिक्त नायट्रोजन आणि ऑक्सिजनचे प्रमाण जास्त हवेच्या प्रमाणावर अवलंबून असते.
1 किलो द्रव इंधनाच्या दहन दरम्यान दहन उत्पादनांचे वस्तुमान (किलोमध्ये)
वायू इंधनाच्या ज्वलनाच्या वेळी दहन उत्पादनांचे प्रमाण निश्चित करूया. वायू इंधनाच्या 1 मोल (किंवा 1 m3) साठी आमच्याकडे वैयक्तिक घटकांची संख्या आहे (मोल किंवा m3 मध्ये)

जेथे N2 हे इंधन, mol किंवा m3 मध्ये नायट्रोजनचे प्रमाण आहे.
जेव्हा 1 मोल किंवा 1 m3 वायू इंधन जाळले जाते, तेव्हा ज्वलन उत्पादनांचे प्रमाण (मोल्स किंवा m3 मध्ये)
सूत्र (50), नंतर
जेथे Mo तीळ किंवा m3 मध्ये आहे.
ते लक्षात घेऊन
आम्हाला मिळते (मोल्स किंवा एम 3 मध्ये)
समीकरणावरून (७४) आपल्याकडे आहे
दर्शविते की हायड्रोजन आणि कार्बन मोनॉक्साईडच्या मोलच्या संख्येचे गुणोत्तर दिलेल्या इंधनासाठी अंदाजे स्थिर आहे आणि a च्या मूल्यावर अवलंबून नाही. द्वारे हे नाते सूचित करूया
अपूर्ण दहन दरम्यान ऑक्सिजनसह कार्बनची रासायनिक अभिक्रिया फॉर्म असते
![]()
ज्वलनात भाग घेतलेल्या ऑक्सिजनच्या तुलनेत ज्वलन उत्पादनांचे प्रमाण 2 पट वाढते.
) उत्पादनांचे प्रमाण
दहन मूल्य (kmol मध्ये)
अपूर्ण ज्वलनाच्या बाबतीत दहन उत्पादनांमध्ये पाण्याच्या वाफेचे प्रमाण समीकरणावरून निश्चित केले जाते.
दहन उत्पादनांमध्ये मुक्त हायड्रोजनचे प्रमाण (kmol मध्ये).
ज्वलन उत्पादनांमध्ये पाण्याची वाफ आणि हायड्रोजनचे एकूण प्रमाण (kmol मध्ये)
हवेतील नायट्रोजन लक्षात घेऊन, समीकरणे (82) आणि (85) (किमीओलमध्ये) पासून ज्वलन उत्पादनांचे एकूण प्रमाण
इंधन वैशिष्ट्याद्वारे [Eq.
कार्बनच्या ज्वलनासाठी आवश्यक प्रतिक्रियेत भाग घेणारे ऑक्सिजनचे प्रमाण
![]()
CO मध्ये कार्बन
हायड्रोजन
![]()
प्रतिक्रियेत एकूण ऑक्सिजनचा समावेश होतो
(८२), (८५) आणि (७९) समीकरणांमधून आपल्याकडे आहे
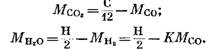
अभिव्यक्ती (92) आणि (93) ला समीकरण (91) मध्ये बदलल्यानंतर, आम्हाला मिळते
ज्वलन उत्पादनांमध्ये समाविष्ट असलेल्या प्रत्येक घटकाचे प्रमाण (kmol मध्ये) खालील सूत्रांद्वारे निर्धारित केले जाते, अनुक्रमे (79), (92), (93) आणि (95) या अभिव्यक्तींमधून प्राप्त केले जाते:
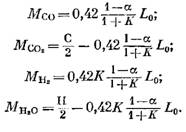
नायट्रोजन रक्कम
![]()
काजळीचे कण हे घन फिल्टर असतात ज्यात मुख्यतः घन कार्बन C असतो.
कार्बनच्या भागातून CO तयार झाल्यामुळे प्रतिक्रियेचा थर्मल प्रभाव कमी होतो. या घटकांची उपस्थिती अत्यंत अवांछित आहे, कारण त्यांच्यात विषारी गुणधर्म आहेत. जेव्हा हे घटक इंजिन सिलेंडरमधून एक्झॉस्ट गॅससह काढले जातात तेव्हा ते हवा प्रदूषित करतात आणि मानवी आरोग्यावर हानिकारक परिणाम करतात. म्हणूनच, अलीकडेच वातावरणात उत्सर्जित होणाऱ्या एक्झॉस्ट वायूंच्या तटस्थतेकडे विशेष लक्ष दिले गेले आहे. ज्वलन उत्पादनांच्या विषारी घटकांमध्ये लीड गॅसोलीनच्या ज्वलनाच्या वेळी तयार होणारे लीड ऑक्साईड देखील समाविष्ट असतात (तक्ता 2 पहा).
अतिरिक्त ऑक्सिजन असतानाही हायड्रोकार्बन्सचे अपूर्ण ज्वलन आणि थर्मल विघटन यामुळे ॲल्डिहाइड्स आणि काजळी निर्माण होते. या घटकांचे प्रमाण मध्यवर्ती रासायनिक अभिक्रियांच्या स्वरूपावर अवलंबून असते.
तथापि, त्याची एकाग्रता तुलनेने कमी आहे.
ज्वलन उत्पादनांमध्ये जवळ-भिंतीच्या झोनच्या उपस्थितीद्वारे स्पष्ट केले जाते “दहन कक्ष मध्ये, जेथे भिंतींशी चार्जच्या संपर्कामुळे, ज्याचे तापमान तुलनेने कमी असते, ज्योत विझते.
ज्या काळात कमी तापमानात ऑक्सिडेशन प्रक्रिया होते त्या काळात अल्डीहाइड्स तयार होतात. ही घटना स्टार्ट-अप दरम्यान, तसेच त्या भागात ऑपरेटिंग मोड्स दरम्यान दिसून येते जेथे ज्वलनाचे मिश्रण तुलनेने थंड पृष्ठभागांद्वारे थंड केले जाते जे दहन कक्ष मर्यादित करते. डिझेल इंजिनमध्ये, जेथे ज्वलन सुरू होण्यापूर्वी लगेच इंधन इंजेक्शन सुरू होते, ज्वलनासाठी हवा-इंधन मिश्रण तयार करताना उद्भवणाऱ्या तथाकथित प्री-फ्लेम प्रतिक्रियांदरम्यान अल्डीहाइड्स तयार होतात (धडा VI पहा). अतिशय पातळ मिश्रणासह डिझेल इंजिनचे ऑपरेशन, जे कमी भारांसाठी वैशिष्ट्यपूर्ण आहे, तसेच गॅसोलीन इंजिनमधील इंधनाच्या शेवटच्या भागाचे ज्वलन, ज्वलन प्रक्रिया आयोजित करण्याची एक विशेष पद्धत (लेयर-बाय-लेयर मिश्रण) निर्मिती) वापरला जातो, ज्यामुळे अल्डीहाइड्स तयार होतात.
चेंबरच्या वेगवेगळ्या भागात
ज्वलनासह, इंधन तुटते आणि कार्बन (काजळी) बाहेर पडतो. कार्बोरेटर इंजिनमध्ये, मिश्रणाची रचना एकसंध (एकसंध) असते आणि सामान्य इंजिन ऑपरेशन दरम्यान काजळी जवळजवळ नगण्य प्रमाणात तयार होते.
इंधन हायड्रोकार्बन्सच्या ऑक्सिडेशनच्या रासायनिक अभिक्रियामुळे तापमान झपाट्याने वाढते अशा ज्वलन कक्षाच्या भागात अणू ऑक्सिजनच्या उपस्थितीत नायट्रोजन ऑक्साईड तयार होतात. नायट्रोजन ऑक्साईडचे प्रमाण ज्वलन उत्पादनांमध्ये नायट्रोजन आणि ऑक्सिजन सामग्रीवर अवलंबून असते.
वायुमंडलीय हवेसह ज्वलन उत्पादनांच्या एक्सचेंज प्रसाराच्या अटींद्वारे निर्धारित केले जाते.
ज्वलन उत्पादनांमध्ये जेव्हा स्पार्क इग्निशन इंजिन लोड आणि निष्क्रियतेशिवाय चालू असते (GOST 1653370) आणि डिझेल एक्झॉस्ट गॅसेसमधील धुराच्या सामग्रीवर (GOST 1902573).
दहन उत्पादनांची रचना. दहन उत्पादनांची रचना निर्धारित करताना कोणत्या आवश्यकता सेट केल्या जातात यावर अवलंबून, योग्य उपकरणे आणि विश्लेषण तंत्र निवडले जातात. गॅस नमुने विश्लेषित करण्याच्या उपकरणे आणि पद्धतींसाठी विशेष साहित्य समर्पित आहे.
अंजीर मध्ये. आकृती 19 डिझेल इंजिन आणि कार्बोरेटर इंजिनच्या एक्झॉस्ट वायूंमध्ये ज्वलन उत्पादनांच्या सामग्रीसाठी वक्र दाखवते. गुणांक a मधील बदल इंजिन लोडवर अवलंबून असतो.
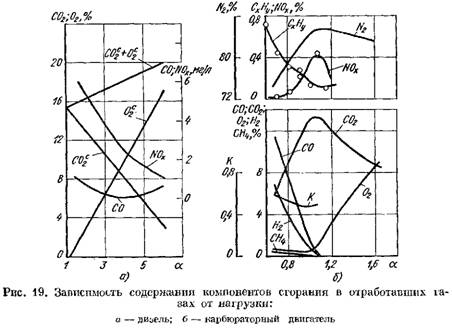
कोरड्या वजनाच्या बाबतीत (चित्र 19, अ)
वाढते.
2 झपाट्याने वाढते आणि दहन उत्पादनांमध्ये कमी प्रमाणात ऑक्सिजन असते ज्याने दहनमध्ये भाग घेतला नाही.
![]() जेव्हा ज्वलन प्रक्रिया बिघडते.
जेव्हा ज्वलन प्रक्रिया बिघडते.